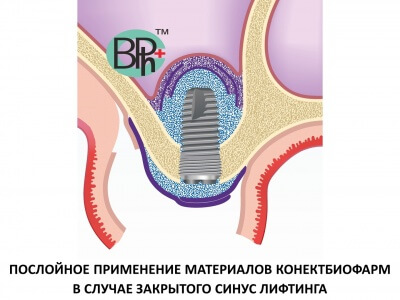
Остеопластические материалы для пародонтологии
Физиологическое уменьшение альвеолярного отростка составляет порядка 0,35-0,39 миллиметра за каждые 10 лет жизни взрослого человека. Такая скорость потери ткани позволяет удерживать зуб в кости челюсти на протяжении всей жизни.
Недостаточная гигиена ротовой полости может приводить к ускорению рассасывания кости до скорости порядка 0,2 миллиметра в год.
Метаболизм в костной ткани тесно связан с механической нагрузкой, стимулирующей ее образование. При наличии дефектов зубного ряда механическая нагрузка на альвеолярную костную ткань существенно снижена или полностью отсутствует.
При потере естественных зубов наблюдается стремительная атрофия альвеолярного отростка, и челюстная кость в данном случае может иметь более плотное строение. Плотность кости вокруг корней ниже в местах, где отсутствуют зубы.
Процесс постэкстракционной атрофии костной ткани протекает относительно быстро, особенно в течение первых 2-3 месяцев после удаления зубов. Степень атрофии достигает впечатляющих значений 40-60% резорбции за 2-3 года. Это происходит вследствие недостаточной нагрузки на альвеолярный отросток.
В дальнейшем, при отсутствии неблагоприятных факторов, процесс резорбции несколько замедляется, и скорость его составляет в пределах 1% каждый год.
Средняя скорость атрофии кости нижней челюсти без зубов составляет в среднем 0,2 миллиметра в год. Это происходит, в первую очередь, за счет ее губчатого вещества. На разных участках челюсти скорость атрофических процессов отличается.
Например, в боковых отделах челюсти атрофия носит более выраженный характер, чем в подбородочном. Это свидетельствует о необходимости поиска новых методов оптимизации состояния костного ложа реципиентов при стоматологическом лечении.
Одним из факторов, которые влияют на состояние кости альвеолярного отростка, является системный остеопороз. В ряде отечественных и зарубежных исследований удалось доказать связь между остеопорозом и степенью уменьшения плотности челюстной кости.
Поскольку такая связь существует, мы можем смело утверждать, что один из факторов, влияющих на состояние альвеолярного отростка — это системный остеопороз.
Особенности остеопластических материалов для пародонтологии
С целью стимуляции восстановления костной ткани и замещения костных дефектов после хирургического вмешательства рекомендуется применение остеопластических материалов различного происхождения и степени обработки.
К ним относят лиофилизированные, формалинизированные, деминерализованные, депротеинизированные препараты кости и хряща, а также брефоматериалы, препараты крови, коллагеновые материалы, аутотрансплантаты, биопластмассы и тканевые трансплантаты.
Перспективным методом местной коррекции метаболических процессов в кости является применение гидроксиапатита (ГАП), оказывающего специфическое остеотропное действие.
Исследования роли цитрата (ЦИТ) и карбоната (КАР) в профилактики и лечения переломов, остеопороза и других видов костной патологии выглядят достаточно перспективно.
Карбонапатит составляет 4% костной ткани, влияет на растворимость и прочности костей человеческого тела. На долю цитрата приходится порядка 1% костной массы. Ионизированный ЦИТ участвует в процессах деминерализации кости.
Цитрат кальция, в свою очередь, принимает участие в минерализации. При помощи меченых атомов доказано, что КАР и ЦИТ служат активными элементами метаболических процессов в кости, как в физиологических, так и в патологических условиях.
Резорбируемая биокерамика
В поисках адекватного остеопластического материала для пародонтологии исследователи обратили внимание на резорбируемую биокерамику. Она представлена гидроксиапатитом и трикальцийфосфатом. Благодаря своим свойствам данная группа веществ стала оптимальным вариантом для остеопластики.
Преимущества резорбируемой биокерамики следующие:
-
Структурное сходство с главным минеральным компонентом костной ткани
-
Способность поддаваться постепенной резорбции
-
Способность выполнять роль матрикса для новой кости
-
Полная биологическая совместимость
-
Отсутствие токсичности
-
Доступность
Более того, местное применение гидроксиапатита и трикальцийфосфата создает благоприятные условия для ремоделирования альвеолярной кости.
ГАП и бета-трикальцийфосфат в пародонтологии используют в форме гранул, порошка, а также в составе композиций. Основное преимущество имплантатов из кальций-фосфатной керамики — это способность образовывать прочные химические связи с костью за счет интенсивного врастания костной ткани реципиента внутрь пористой структуры.
Применение гидроксиапатита при дефектах тканей пародонта оптимизирует процессы остеогенеза и цементогенеза, способствует образованию полноценного зубо-десневого прикрепления. Однако исследования ряда авторов показали, что рентгенологически новообразованная кость в присутствии ГАП остается плохо структурированной, отличающейся от окружающей естественной кости.
Разработчики остеопластических материалов на основе гидроксиапатита высокой дисперсности объясняют это тем, что авторы использовали малоактивные с биохимической точки зрения композиции. По мнению заинтересованных представителей индустрии, ГАП высокой дисперсности имеет оптимальные биомеханические свойства.
Синтетические остеотропные керамические материалы российского и зарубежного производства приобрели широкое распространение в стоматологической практике.
Современные синтетические остеопластические материалы характеризуются:
-
Высокой механической прочностью
-
Биологической совместимостью
-
Отсутствием мутагенных свойств
-
Низкой аллергенностью
-
Апирогенностью
Биологически активные вещества в составе указанных продуктов способствуют достижению оптимального терапевтического эффекта. Кроме того, большинство материалов на основе ГАП и бета-трикальцийфосфата легко формуются в полостях со сложным рельефом.
Практика отсроченной имплантации с использованием остеотропной биокерамики показала, что эти материалы обладают высокой эффективностью и существенно расширяют показания дентальной имплантации. Однако эта группа продуктов не лишена ограничений.
Из недостатков стоит упомянуть, что они не оказывают выраженного остеоиндуктивного эффекта, требуемого от современных материалов для пародонтологического лечения.
В России и за рубежом предпринимались попытки усовершенствовать эту группу путем добавления специфических компонентов с противовоспалительными, бактерицидными или иными свойствами. Например, композиции с антисептиком диоксидином.
Для материалов из стеклокерамики характерно отсутствие иммунологической активности. В значительной мере высокая биосовместимость объясняется тем, что элементарный состав их является приближенным к натуральному. Такие остеопластические материалы создают оптимальные условия для восстановления тканей пародонта.
Введение в костные карманы пластичного материала предотвращает вегетацию эпителия десневого края внутрь в направлении апикальной части корня зуба. Это приостанавливает доступ ротовой жидкости и микрофлоры, снижая вероятность осложнений.
Аутотрансплантаты в пародонтологии
Благодаря оптимизации процесса репаративного остеогенеза внимание исследователей привлекают аутотрансплантаты, обладающие высоким остеогенным потенциалом.
В клинической практике признано, что аутогенный костный трансплантат в значительной мере способствует быстрому замещению послеоперационных и других костных дефектов новообразованной костью. Он отличается пластичностью и полностью исключает иммунологическую несовместимость с организмом реципиента.
Однако, наряду с этими важными преимуществами, аутотрансплантат имеет существенные недостатки, которые ограничивают его использование в клинической практике:
-
Травматичность получения материала
-
Физически ограниченный источник ткани
-
Инфекции и другие осложнения
В связи с этим для восстановления альвеолярного отростка чаще используются ксеноматериалы и различные виды аллотрансплантатов.
При использовании деминерализованного аллогенного остеопластического материала происходит запуск остеоиндуктивного механизма, направленного на дозревание популяции остеогенных клеток и их пролиферацию. Экспериментально-клинические исследования демонстрируют его существенные преимущества перед замороженными или формалинизированными аллогенными материалами.
С другой стороны, существуют технические и организационные трудности получения данных материалов. Не исключается угроза иммунного конфликта. Деминерализованный аллогенный материал для остеопластики сложнее использовать по причине меньшей стойкости к инфекциям по сравнению с синтетическими аналогами.
При проведении лоскутных операций было предложен комбинированный трансплантат оригинального состава. Он состоит из аллогенной костной муки, которая консервируется при низкой температуре, сорбционно-противомикробного комплекса, фуразолидона, метронидазола. Порошок замешивается с желе активегина до консистенции пасты.
Ксеногенные остеопластические материалы
Ксеноматериалы считаются одними из наиболее перспективных для остеогенеза.
Основной их составляющей является коллаген, который активно участвует в обменных и регенеративных процессах в соединительной ткани. Коллаген способствует улучшению ее механической, пластической и защитной функции.
Коллагеновые материалы способны резорбироваться в тканях и стимулировать регенеративные процессы, в том числе в кости. При этом они не облагают мутагенными, канцерогенными и токсическими свойствами, а их антигенность считают минимальной.
Чаще всего в клинической практике применяют ксеногенные материалы из бычьей кости, которая подвергается специальной высокотехнологичной обработке — депротеинизации. В результате устраняется антигенное влияние ксеноматериала в тканях организма.
После обработки ксеноматериалы становятся, по сути, костными минералами. Они могут поглощаться и рассасываться, но при этом лишены остеоиндуктивных свойств. В то же время ксеноматериалы являются остеокондуктивными агентами. В результате их действия и реакции окружающих тканей происходит активное костное прорастание.
Развитие кости направляется от ложа ксенотрансплантата с депонированием костных клеток на его поверхности. Сам материал в процессе костного прорастания подвергается резорбции и реконструкции с последующей заменой на полноценную костную ткань.
Направленная регенерация тканей
Новые возможности в пародонтологии и дентальной имплантации открывает современная технология под названием направленная регенерация тканей. Она основывается на сложной взаимосвязи кроветворения и процессов образования новой кости.
В направленной регенерации принимают участие ключевые элементы костномозгового кроветворения, кислородозависимые элементы костного мозга и костной ткани пародонта, многообразные гуморальные и тканевые факторы.
Данный метод позволяет не только восстановить альвеолярный отросток, но и достичь полноценной регенерации других частей пародонта — периодонтальной связки и корневого цемента. Образование последнего происходит в фазе конструирования костного матрикса.
Клетки-предшественники цементобластов располагаются в жизнеспособном периодонте и костномозговых пространствах. В процессе регенерации основное вещество цемента пропитывается солями кальция, а коллагеновые волокна соединяются с аналогичными волокнами альвеолярного отростка, пребывающего в процессе регенерации.
Восстановление волокон периодонта происходит за счет жизнеспособных фибробластов сохранившейся периодонтальной связки. Использование мембран дают возможность медленно растущим клеткам периодонтальной связки распространиться на поверхность корня, создав таким образом условия для регенерации пародонта в целом.
Мембраны для направленной регенерации позволяют частично закрывать фуркационные и вертикальные костные дефекты, в некоторой степени увеличивать прирост ткани альвеолярного отростка, а также устранять рецессию мягких тканей.
Основным недостатком данного подхода является незначительный объем хирургического вмешательства (не более двух зубов) в связи с тем, что при расширении объема вмешательства возможно нарушении трофики регенерирующих тканей.
Остается открытым вопрос, как исключить типичные осложнения — например, коллапс мембраны. Среди минусов метода стоит упомянуть высокую стоимость операций.
Применение остеотропных средств в пародонтологии
Зависимость состояния ткани пародонта от общего состояния костной системы объясняет целесообразность использования системных остеотропных препаратов, которые подавляют процесс резорбции кости. К этим препаратам относят:
-
Препараты кальция
-
Средства заместительной гормональной терапии
-
Витамин D и поливитамины
-
Кальцитонины
-
Бифосфонаты и др.
Кроме того, имеются данные об успешном применении препаратов, которые непосредственно стимулируют образование костной ткани:
-
Иприфлавоны
-
Анаболические стероиды
-
Фториды и др.
Препараты антирезорбтивного действия стимулируют костный метаболизм, тормозят повышенную резорбцию кости, способствуют формированию новой костной ткани в организме в целом и в альвеолярном отростке в частности.
Использование этой группы препаратов в пародонтологической практике обусловлено оптимизацией остеопластических процессов в альвеолярном отростке.
Для лечения остеопороза ранее был предложен кальцитонин. Экспериментально установлено, что препарат кальцитонина «Миакальцин» сокращает риск переломов позвоночника на 37,4%. Миакальцин оказывает системное действие.
При лечении индуцированного кортикостероидами или постменопаузального остеопороза широко применяются препараты группы бифосфонатов. Хорошие результаты при лечении генерализованного пародонтита у женщин в постменопаузе показал алендронат.
Бифосфонаты приводят к выраженному замедлению патологических процессов при остеопорозе и приостанавливают резорбцию альвеолярной кости.
Золотым стандартом антирезорбтивной терапии долгое время считается комбинация препаратов кальция, бифосфонатов, кальцитонина и женских половых гормонов. Эта комбинированная терапия рекомендуется для лечения и профилактики остеопороза.
Препараты кальция используются при заболеваниях пародонта. Они считаются необходимыми, если заболевание протекает на фоне нарушения обменных процессов в костной ткани, поскольку существует прямая связь между уменьшением плотности опорной кости и дистрофическими резорбтивными процессами в альвеолярном отростке.
Назначение препаратов кальция настоятельно рекомендуется при лечении заболеваний пародонта, поскольку при ряде нарушений обмена веществ в костной ткани увеличивается выведение кальция почками и слюнными железами. Однако получить хорошие долгосрочные результаты можно только при использовании тщательно продуманной комбинации препаратов кальция с другими остеотропными средствами.
В частности, для профилактики и лечения остеопороза зарубежными авторами были предложены биологически активные продукты, основанные на протеинах, витаминах D, E, C, A с различным содержанием кальция, микро- и макроэлементов. Некоторые клинические исследования подтверждают эффективность таких продуктов в комплексном лечении генерализованного пародонтита.
Комбинированные остеотропные средства на основе кальция:
-
Замедляют развитие остеопороза
-
Улучшают структурно-функциональные свойства альвеолярного отростка
-
Повышают минеральную плотность костей по всему организму
Классическим препаратом для замедления резорбтивных процессов альвеолярной кости считается аналог витамина D – альфакальцидол — внесенный в 2012 году в российский перечень жизненно важных лекарственных средств (ЖНВЛП).
Хорошо известными средствами для лечения и профилактики остеопороза являются препараты фтора, который накапливается преимущественно в костях и зубах. Фтор в костном матриксе служит биокатализатором процессов минерализации и регулятором метаболизма.
По этой причине препараты фтора незаменимы в комплексном лечении пациентов с общими остеопоротическими изменениями, помимо проблем со стороны тканей пародонта.
Заключение
Использование остеопластических материалов для пародонтологии — перспективное направление, наряду с развитием новых системных остеотропных препаратов.
Успех такого лечения требует тщательной оценки состояния здоровья пациента, а также наличия необходимых технических и материально-финансовых возможностей.