Костные материалы для мастоидопластики
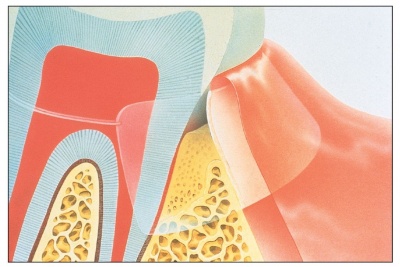
Анатомическое строение сосцевидного отростка и барабанной полости оказывает серьезное влияние на характер течения среднего отита.
Важнейшей задачей хирургического лечения является ликвидация воспалительного процесса в полости среднего уха и максимальное приближение анатомического строения оперируемого уха к норме путем пластических операций, в том числе с применением костных материалов.
Хирургические вмешательства открытого типа являются нефизиологичными, поскольку нарушается архитектоника среднего уха, а в эпидермальном покрове трепанационной полости сохраняются патоморфологические признаки ранее перенесенного хронического гнойного среднего отита (ХГСО), независимо от качества проведенной операции.
Трепанационная полость, образованная в результате вмешательства, в течение полугода не заживает у 20% оперированных больных, а гноетечение продолжается почти у трети пациентов. Скопление эпидермальных масс в послеоперационной полости способствует обострению хронического воспалительного процесса.
Морфологические изменения в мастоидальной полости классифицируют как «болезнь трепанационной полости» или «болезнь оперированного уха».
У данной категории больных отмечается ухудшение звукопроведения в диапазоне 0,5-4 кГц в среднем на 15 дБ по сравнению с пациентами, у которых задняя стенка наружного слухового прохода была сохранена или восстановлена.
Потеря слуха находится в прямой зависимости от объема трепанационной полости. У пациентов после санирующих вмешательств открытого типа возникают затруднения в процессе проведения слухокорректирующих операций, а также при подборе слухового аппарата.
Санирующие операции закрытого типа с сохранением или с последующим восстановлением задней костной стенки наружного слухового прохода без выполнения мастоидопластики приводят к рубцовому заживлению послеоперационных костных полостей, что является нефизиологичным.
У этой категории больных может возникать воспалительный процесс и рецидив холестеатомы в антромастоидальном пространстве (до 40% взрослых и 67% детей), что отрицательно влияет на функциональное состояние слуховой трубы.
При одновременно проводимых санирующих операциях с тимпанопластикой у 55-63% таких пациентов, по данным разных авторов, возникают ретракционные карманы.
Санирующие операции с сохранением или реконструкцией задней стенки наружного слухового прохода и облитерацией мастоидальной полости являются эффективными, и позволяют достичь устойчивого санирующего результата в 89-100% больных, оперированных по поводу ХГСО.
В этих случаях при одновременном проведении санирующей операции и тимпанопластике отсутствует риск развития ретракционных карманов. Описанная выше операция считается оптимальным методом реабилитации пациентов с «болезнью трепанационной полости».
В сочетании с тимпанопластикой проведение такого хирургического вмешательства позволяет достичь полной реабилитации у данной категории больных.
В связи с этим особое значение приобретает мастоидопластика, направленная на ликвидацию послеоперационной полости. Идеальным костным материалом для мастоидопластики принято считать аутогенные костные трансплантаты, которые имеют высокие остеогенные свойства, однако их не всегда достаточно для закрытия дефекта.
Поэтому ведется поиск альтернативных костно-пластических материалов, которые могли бы решить данную проблему заживления костного дефекта новообразованной костной тканью, не причиняя пациенту дополнительной травмы при получении аутокости.
Применение мягких тканей и костных материалов для мастоидопластики
Стремление уменьшить объем трепанационной полости послужило причиной разработки различных способов мастоидопластики, направленных на ликвидацию мастоидальной полости.
Принцип мастоидопластики заключается в ликвидации трепанационной полости в сосцевидном отростке путем заполнения ее различными трансплантатами: костными, хрящевыми, мышечными тканями, аллопластическими костными материалами и др.
Эта операция является завершающим этапом санирующих хирургических вмешательств на среднем ухе. В некоторых случаях она проводится больным, ранее перенесшим радикальную операцию (так называемая вторичная мастоидопластика).
С момента своего возникновения и до настоящего времени мастоидопластика производится с помощью свободно пересаживаемых трансплантатов и трансплантатов на ножке.
В качестве биологических трансплантатов для мастоидопластики использовались различные ткани. Применение жировой ткани в качестве материала для заполнения костного дефекта имеет такие существенные недостатки, как опасность некроза тканей.
Кроме того, в полости происходит трансформация свободно пересаженного жирового лоскута в рубцовую ткань, что ведет к повторному появлению полости в сосцевидном отростке и во многом способствует втягиванию кожи задней стенки наружного слухового прохода в сторону мастоидальной полости.
Монтадор и соавторы в 1995 описали применение для мастоидопластики жировой ткани, предварительно восстанавливая заднюю стенку наружного слухового прохода с помощью резицированной задней костной стенки при санирующей операции.
С конца 1960-х по середину 1970-х годов некоторые отохирурги активно применяли для мастоидопластики кровяной сгусток. Однако в результате ферментативного расплавления кровяной сгусток крови частично замещался соединительной тканью.
В дальнейшем рубцовое преобразование соединительной ткани вело к повторному появлению полости. Нередко наблюдалось нагноение, так как кровь является хорошей питательной средой для большинства патогенных микроорганизмов.
Для мастоидопластики используется также височная мышца на питающей ножке. Данный метод мастоидопластики был предложен Рэмбо в 1957 году, и получил название мускулопластики.
Хильгер и Хольманн в 60-х годах прошлого столетия для заполнения мастоидальной полости формировали лоскуты из височной и заушной мышц. Также для облитерации мастоидальной полости применяли свободную аутопластику мышечной тканью.
Айзенберг в 1966 использовал для мастоидопластики кашицу из мышечной ткани.
В свою очередь, Богданова применяла измельченную мышечную ткань с добавлением осколков кости, полученных в ходе снятия кортикального слоя сосцевидного отростка.
Как отмечала автор, использование измельченной мышцы для мастоидопластики нерационально, поскольку превращение ее в рубцовую ткань в отдаленные сроки после операции сопровождалось резким уменьшением первоначального объема.
Новообразования костной ткани в мастоидальний полости Богданова не наблюдала.
Некоторые отохирурги заполняли трепанационную полость лоскутами на толстой и короткой ножке, взятыми из заушной области, которые состояли, главным образом, из мышечной ткани.
Для заполнения костных полостей сосцевидного отростка большое распространение получили мягкотканные трансплантаты, главной составной частью которых была мышечная ткань.
Активно применялся мышечно-периостальный лоскут, сформированный из тканей заушной области на двух или одной питательной ножке, в комбинации с хрящом и силиконовым блоком, хрящом, аутокостью и др. Известны техники использования мышечно-фасциально-периостального лоскута, предварительно обработанного антибиотиком, а также височно-фасциально-периостального и височно-теменно-фасциального лоскута.
Некоторые отохирурги с целью уменьшения объема трепанационной полости применяют мышечно-периостальный лоскут. Заушная рана ведется открытым путем и постепенно облитерирует благодаря разрастанию в ней рубцовой ткани.
По информации разных источников, после применения данного пластического материала в 10-18% случаев отмечалось сужение наружного слухового прохода и выраженная оторея, атрофия мышечно-периостального трансплантата и дальнейшая резорбция, а также вовлечение кожи заушной области с образованием косметического дефекта.
Как показал клинический опыт, мышечный лоскут имеет ряд недостатков. Его получение связано с причинением пациенту дополнительной травмы и с опасностью развития в послеоперационном периоде гематом и невралгии в области хирургического вмешательства.
Нерифилд в 1963 году после мастоидопластики с использованием мышечной ткани в отдаленном послеоперационном периоде наблюдал абсцесс мозга. Некоторые авторы отмечали сужение просвета наружного слухового прохода вследствие отека мышечного лоскута, что в послеоперационном периоде усложняло уход за барабанной полостью.
В отдаленном периоде, в результате преобразования мышечного лоскута в рубцовую ткань, у пациентов наблюдалось нежелательное увеличение объема мастоидальной полости. У 17-25% таких больных в послеоперационном периоде образовывались обширнейшие полости с разрастанием грануляций и возобновлением гноетечения.
Нередко наблюдалось инфицирование раны в результате некроза мышечного лоскута.
В 1972 году Вулштейн и соавторы использовали для пересадки, особенно при небольших полостях, свободные лоскуты с фасции височной мышцы либо периоста и соединительной ткани сосцевидного отростка. Для мастоидопластики применялся также соединительнотканный лоскут на питающей ножке, выкроенный с заушной области.
Овсянников в 1969 использовал для заполнения мастоидальной полости соединительнотканно-мышечно-костный и соединительнотканно-мышечный лоскуты. Соединительнотканный лоскут для трансплантации применяли Андрейчук, Тарасюк и другие отечественные авторы.
Многие отохирурги выполняли мастоидопластику с использованием мягких тканей, полученных из заушной области, адаптируя различные варианты операции. После заполнения мастоидальной полости мягкотканными аутотрансплантатами гноетечение прекращалась у 75-80% больных.
Следует отметить, что в отдаленном периоде после облитерации антромастоидальной полости мягкими трансплантатами у больных, которым во время санирующей операции была сбита задняя костная стенка наружного слухового прохода, часто возникал рецидив трепанационной полости.
В связи с наблюдаемым вовлечением кожи задней стенки наружного слухового прохода, дальнейшее совершенствование мастоидопластики было направлено на сохранение и задней костной стенки наружного слухового прохода во время санирующей операции.
Так, Ханамиров (1966) и Овсянников (1975) выполняли мастоидопластику мягкими тканями, сохраняя при этом всю или большую часть костной стенки наружного слухового прохода.
Сегодня для реконструкции задней стенки наружного слухового прохода используют:
· реберный аутохрящ
· аутохрящ перепонки носа
· хрящ козелка или ушной раковины с кортикальной аутостружкой
· губчатую кость с костным мозгом, полученную из подвздошной кости больного
· расщепленный мышечно-периостальный лоскут и др.
Как свидетельствуют данные литературы, использование мягкотканных трансплантатов малоэффективно, поскольку у 15-20% пациентов отмечается продолжение гноетечения, почти у каждого третьего трансплантаты подвергаются некрозу и отторгаются, часто возникают осложнения в участке выкраивание лоскута.
Мягкие ткани не является специфическими стимуляторами остеогенеза, а некоторые из них негативно влияют на этот процесс. Кроме того, мягкотканные лоскуты трансформируются в рубцовую ткань, уменьшаются в объеме, ведут к рецидиву мастоидальной полости.
Линтикум в 2002 году сравнивал такие пластические материалы для мастоидопластики, как жировая ткань, костная стружка, костная мука, подкожные ткани, мышцы. Автор сделал вывод: жировая и костная ткань (костная стружка или костная мука) сохраняют свой объем в облитерированной полости, тогда как подкожная ткань и мышцы теряют его.
Абдельрахман и соавторы в 2008 году также отметили, что костная стружка в послеоперационном периоде сохраняет свой исходный объем в облитерированных полостях и со временем замещается новообразованной костной тканью.
Анализ литературы, содержащей результаты клинических и экспериментальных исследований, показывает, что мастоидопластика с применением мягкотканных трансплантатов не влечет к ликвидации трепанационной полости в сосцевидном отростке.
Для облитерации антромастоидальной полости применялись хрящ ушной раковины, реберный хрящ или же реберный хрящ в комбинации с кортикальной аутостружкой, формалинизованный хрящевой аллотрансплантат.
При трансплантации хряща в мягкие ткани последние способствовали сохранению его структуры, тогда как при пересадке в костную полость происходило замещение хряща костной тканью.
Мастоидопластика лиофилизированным хрящевым аллотрансплантатом описывается в исследованиях Андрийчука.
Гейне и соавторы в 1976 применяли для заполнения костной полости сосцевидного отростка хрящевой аутотрансплантат или аллотрансплантат носовой перегородки. У четверти пациентов параллельно с мастоидопластикой проводилась и реконструкция задней костной стенки наружного слухового прохода.
Осложнений, связанных с облитерацией костного дефекта и восстановлением задней костной стенки наружного слухового канала, авторы не наблюдали.
Меланин для мастоидопластики также использовал реберный или четырехугольный хрящ носовой перегородки, консервированные в 0,5% растворе формалина.
Наблюдение за 8 пациентами в отдаленном послеоперационном периоде выявило у шести человек полную облитерацию трепанационной полости, у одного отмечалось почти полное восстановление полости, еще у одного – частичное.
Во время реоперации, проведенной через 1 год, мастоидальная полость была выполнена фрагментами хряща, которые сохранили свои первоначальные размеры. В промежутках между пересаженным хрящом находилась соединительная ткань, плотно спаяна с трансплантатом, а некоторые хрящевые фрагменты частично оссифицировались.
Проведенные Богдановой и Бланк (1975) рентгено-томографические исследования показали, что при применении измельченного хрящевого аллопластического материала у 11 больных, в 4 случаях, где трепанационного полость была небольшой, хрящевая ткань замещалась костной тканью, у остальных новообразования костной ткани не произошло.
При повторной операции у троих пациентов, у которых для мастоидопластики использовался хрящевой аллотрансплантат, наряду с частичной оссификацией хрящевых фрагментов определялась инкапсуляция и разрастание соединительной ткани.
Запорощенко (1988) изучил в сравнительном аспекте репаративные процессы, протекающие в булле кошки после заполнения ее брефоаллотрансплантатом и хрящевым аллотрансплантатом.
Результаты проведенных экспериментальных исследований показали, что при пересадке хряща в костную полость происходит полноценное замещение трансплантата костной тканью. Но автор отметил, что замещение кости плода новообразованной костью реципиента происходило в более ранние сроки, чем замещение хряща, взятого у взрослого донора – это свидетельствовало о выраженных биологических свойствах костного брефоаллотрансплантата.
Экспериментальные исследования Йенга и соавторов (2010) на буллах кроликов продемонстрировали, что гистологические изменения в ходе регенерации хряща напоминают процессы заживления костных переломов. Хрящевая ткань проходит процесс оссификации и трансформируется в костную ткань.
Таким образом, данные литературы свидетельствуют о том, что измельченный хрящевой аллотрансплонтат в небольших костных полостях способен замещаться костной тканью, в некоторых случаях он рассасывается.
Чаще же происходит инкапсуляция в соединительной ткани с частичной оссификацией.
С точки зрения стимуляции остеогенеза, оптимальным костным материалом для ликвидации дефектов является собственная костная ткань. Аутогенные костные трансплантаты считаются золотым стандартом в остеопластических операциях.
Они имеют высокие остеогенные, остеокондуктивные и остеоиндуктивные свойства. Пересаженный в полость, костный трансплантат замещается новообразованной костью, что приводит к заращению костного дефекта. Проведенные клинические наблюдения показали, что облитерация мастоидальной полости костной пылью или стружкой с точки зрения функционального эффекта лучше, чем облитерация хрящевой тканью.
Костный материал позволяет создать условия для санирующего эффекта и сокращает вероятность таких нежелательных явлений после общеполостных операций, как гноетечение, боль в мастоидальной полости, головокружение, скопление серно-эпидермальных масс.
Некоторые отохирурги для облитерации мастоидальной полости после радикальной операции использовали кортикальную стружку аутокости или костную муку, взятые вокруг мастоидальной полости, сверху которой заключалась височная мышца, мышечно-периостальный лоскут, периостальный лоскут в комбинации с жировой тканью.
В отдаленном периоде отмечали полную облитерацию мастоидальной полости костной тканью.
Чернуха и Горбачук в качестве аутологичного костного материала для мастоидопластики использовали костную стружку кортикально-склерозированного слоя сосцевидного отростка.
Шиллер и коллеги (1960) заполняли мастоидальную полость костными столбиками, полученными из крыла подвздошной кости; этот материал использовали Диденко и Гусакова.
Богданова и Бланк в 1975 предложили заполнять трепанационную полость фрагментами аутологичной кости, полученной из кортикального слоя при подходе к патологическому очагу.
Зберовская применяла лиофилизированный костный аллотрансплантат. Однако применение лиофилизированного костного аллотрансплантата, по мнению исследователя Полежаева, является малоэффективным вследствие снижения биологических свойств костной ткани при консервации.
Меланьин для облитерации трепанационной полости сосцевидного отростка использовал формалинизованный костный аллотрансплантат, полученный из гребня подвздошной кости или костей свода черепа взрослых доноров. Как отмечают авторы, данный метод мастоидопластики является эффективным, так как за1,5-2 года наблюдается полная перестройка трансплантата.
Запорощенко для облитерации мастоидальной полости применял кость свода черепа плода, однако данный костный материал признан труднодоступным и малопригодным вследствие определенных этических и юридических проблем.
По данным зарубежных авторов, хорошие клинические результаты дает использование аллогенных губчатых чипсов, а также современных ксеногенных костных материалов.
Хотя литературные данные свидетельствуют о том, что с точки зрения стимуляции процессов остеогенеза лучшим материалом для мастоидопластики является костный аутотрансплантат, он далеко не всегда имеется в достаточном количестве.
Забор необходимого количества аутокости влечет за собой дополнительную травму и соответствующий дефицит кости в донорском участке.
Кроме того, в послеоперационном периоде возможны различные осложнения.
Указанные обстоятельства подталкивают клиницистов к поискам альтернативных костно-пластических материалов, способствующих заживлению дефекта новообразованной костной тканью, не причиняя пациенту дополнительной травмы.
В свете этого более доступные, безопасные и технологичные аллогенные или ксеногенные костные материалы для мастоидопластики продолжат играть важную роль.