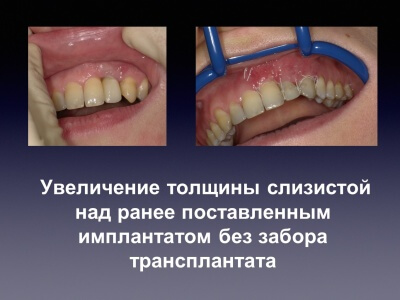
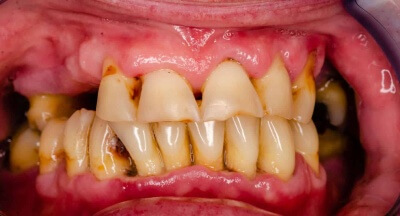
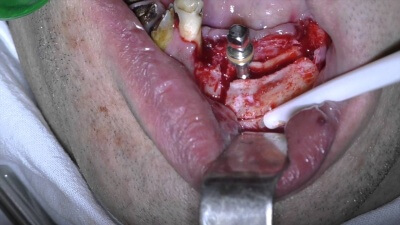
Остеопластические материалы для хирургического лечения генерализованного пародонтита

С целью эффективного влияния на различные звенья патогенеза генерализованного пародонтита (ГП) для достижения стабилизации патологического процесса в пародонте необходима комплексная терапия.
Она предусматривает воздействие на местные и системные факторы, в первую очередь, с помощью консервативных (мануальных и медикаментозных) мер, особенно эффективных в случае начального заболевания и I степени развития генерализованного пародонтита.
По мере углубления тяжести болезни консервативные методики не дают выраженного эффекта, поэтому подключается хирургическое лечение.
Оперативное лечение тканей пародонта включает:
-
Основные операции (проводятся непосредственно на деснах или альвеолярном отростке: разновидности кюретажа, гингивотомия и гингивэктомия, разновидности лоскутных операций).
-
Вспомогательные операции (френуло- и вестибулопластика, вскрытие соединительнотканных тяжей, углубление преддверия полости рта).
Известно, что уже в возрасте 18-34 лет хирургического лечения ГП требует 13,8% больных, у 34-44-летних - 35,4%, в возрасте 45 лет и старше — 40%.
Другие исследователи утверждают, что хирургического лечения требуют порядка 78% пародонтологических больных, причем 68% этих пациентов необходимо проведение лоскутных операций.
У больных ГП II-III степени без хирургического вмешательства зачастую вообще невозможно достичь полного успеха, поскольку только операция позволяет достичь ликвидации очага воспаления, устранить пародонтальные карманы, приостановить деструкцию кости и обеспечить длительную стабилизацию заболевания.
Итак, в комплексном лечении генерализованного пародонтита II-III степени тяжести хирургические методы играют ведущую роль.
Наиболее эффективными при ГП II-III степени считаются лоскутные операции, которые являются вершиной пародонтальной хирургии благодаря возможности:
-
Под контролем провести кюретаж пародонтальных карманов.
-
Удалить поддесневой зубной камень и грануляционную ткань.
-
Выровнять и обработать поверхность костной ткани.
-
Иссечь вросший в карманы эпителий.
Лоскутные операции подразделяются на сугубо лоскутные (вмешательство без подсадки в костные карманы остеопластических материалов) или же операции с использованием стимуляторов репаративного остеогенеза (гингивопластика).
Классическую лоскутную операцию впервые, независимо друг от друга, предложили хирурги Цешинский (1914), Видман (1918) и Нейман (1920).
Процедура включала механическую обработку корней зубов, удаление грануляционной ткани, мобилизацию слизисто-надкостничного лоскута и наложение швов в каждом межзубном промежутке.
Однако из-за сокращения надкостницы часто прорезывались швы, вызывая развитие рецидивов, а в дальнейшем — выраженную ретракцию десен.
Кроме рецессии десны и обнажения корней зубов после заживления раны и связанной с этим повышенной чувствительности зубов недостатком операции является отсутствие восстановления объема костной ткани.
В дальнейшем лоскутную операцию модифицировали с помощью:
-
наложения периостальных швов;
-
частичного расщепления лоскута;
-
использования расщепления лоскутов;
-
увеличения вертикальных разрезов переходной складки и иссечения патологических тканей на 3-4 мм ниже десневого края;
-
отслаивания слизисто-надкостничного лоскута с деэпителизацией внутренней его поверхности фрезой и последующей остеопластикой лиофилизированной костной мукой на крови пациента с добавлением антибиотиков и использованием защитной десневой повязки.
Однако каждый из названных вариантов операции имеет ряд недостатков.
Профессор Владимир Исидорович Лукьяненко в 1977 сумел удачно модифицировать классическую лоскутную операцию Цешинского-Видмана-Неймана. Он дополнил ее проведением горизонтальных разрезов надкостницы одновременно как с вестибулярной, так и с оральной стороны под 35º и сохранением конфигурации десневого края.
Немодифицированные лоскутные операции устраняют воспалительные явления, стабилизируют патологический процесс в пародонте, однако не обеспечивают необходимую регенерацию кости альвеолярного отростка.
Это побудило исследователей к поиску остеопластических материалов с целью стимуляции репаративного остеогенеза после введения в костные дефекты.
Выбор остеопластических материалов для лечения генерализованного пародонтита
Теоретическим основанием применения остеопластики служит установленное нарушение гистофункциональной корреляции зуба с окружающими тканями, в том числе с системой микроциркуляции.
Следовательно, при лоскутных операциях в костные дефекты целесообразно вводить остеопластические материалы.
Материалы для восстановления тканей пародонта по происхождению:
-
Аутогенные внутриротового и внеротового происхождения, которые оказывают выраженное остеоиндуктивное действие.
-
Аллогенные: консервированные материалы от донора-человека.
-
Ксеногенные: полученные от животных путем депротеинизации.
-
Аллопластические: синтетического происхождения.
В качестве аутотрансплантата используются кости черепа, ребра, гребня подвздошной кости, а также костный мозг со стволовыми клетками.
Аутологичный трансплантат впервые применил Megedus (1923), в дальнейшем костную стружку с успехом использовали Forsberg (1956) и Elegaаrd (1976).
Аутотрансплантат имеют ряд клинических преимуществ:
-
Биосовместимость.
-
Биологическая безопасность.
-
Репаративный потенциал.
Существенным недостатком аутокости при лечении костных дефектов считается возможность быстрой резорбции трансплантата в динамике, а также необходимость дополнительного травматичного для пациента вмешательства.
Из-за этого существует риск инфицирования участка-донора, дополнительная операционная кровопотеря, увеличение продолжительности послеоперационного периода.
Несмотря на недостатки, продолжаются исследования по использованию выращенной в толще подвздошной кости аутокости, имеющей структуру гиалинового хряща и грубоволокнистой костной ткани, хрящевых ауто- или гомотрансплантатов, кортикально-губчатых трансплантатов с надкостницей, костно-хрящевых аутотрансплантатов.
Аутокость используют в свежем либо замороженном виде.
В реконструктивной хирургии альвеолярного отростка челюстей при ГП используют ксеногенные и брефокостные трансплантаты, консервированные различными способами: замороженные, формализованные, лиофилизированные, деминерализованные.
Они восстанавливают анатомическую форму отростка, индуцируют остеогенез.
При радикальной гингивоостеопластике используют костные аллотрансплантаты, консервированные в 0,5% растворе формалина.
Их использование сопряжено с риском передачи вирусной инфекции, а также проявлением антигенных свойств и слабым остеоиндуктивным действием.
В случае хирургического лечения генерализованного пародонтита с успехом применяют различные комбинации остеопластических материалов:
-
Консервированный аллогенный костный мозг с костной стружкой.
-
Формалинизированный аллотрансплантат с пентоксифиллином.
-
Аллогенный имплантат из деминерализованной лиофилизированной кости с аутогенным костным материалом.
-
Смесь костного мозга пациента с коллагеновой губкой.
Как трансплантационный материал можно также вводить плацентарную ткань человека, которая стимулирует остеогенез, оказывает противовоспалительное, гемостатическое, антибактериальное действие, а также обладает низкой антигенной активностью.
Также используются ксеногенные материалы животного происхождения, включая такие экзотические продукты, как сублимированная ксенобрюшина, лиофилизированные гиалиновые хрящи крупного рогатого скота с кровоостанавливающим и противовоспалительным действием.
Однако использование ксенотрансплантатов может сопровождаться отторжением материала в результате иммунологической несовместимости, а также сопряжено с теоретическим риском передачи прионных заболеваний.
При операциях на пародонте применяют комбинированные остеопластические материалы, содержащие природные вещества-стимуляторы остеогенеза. Среди них как органические, так и минеральные компоненты костной ткани (гидроксилапатит кальция биологического происхождения).
Ведутся исследования по клиническому использованию гидроксиапатита в комбинации с культурой аутофибробластов, основы клеточного компонента соединительной ткани человека.
На современном этапе развития стоматологии в пародонтальной хирургии новым направлением является тканевая инженерия — использование клеточных технологий формирования живых эквивалентов ткани in vitro с последующим переносом продукта in vivo в клинических условиях.
Несмотря на положительные свойства ауто-, алло- и ксеногенных остеопластических материалов, их ограничения привели к разработке альтернативных неорганических и органических синтетических материалов: гидроксиапатит, α- и β-трикальцийфосфат, биоактивное стекло, сульфат кальция, карбонат кальция, синтетические полимеры и биокерамика.
Перспективным направлением в пародонтальной хирургии стало использование остеопластических материалов на основе коллагена, насыщенных сульфатированными гликозаминогликанами (сГАГ).
Новые пластические биоматериалы с низкой токсичностью и антигенностью и высокой механической прочностью и устойчивостью к тканевым протеаз могут интегрироваться в ткани пародонта без фиброзного перерождения и способствуют быстрой регенерации костной ткани.
Для лечения костных дефектов при генерализованном пародонтите успешно применяют «Биоимплант ГАП» - это неорганический матрикс бычьей кости с сохранением природной архитектоники костной ткани.
«Биоимплант ГАП» способствует формированию в дефекте собственной костной ткани, а после восстановления рассасывается. Продукт используется в сочетании с другими биоматериалами и биоактивными веществами, коллагеновой мембраной «Биоматрикс» и др.
Материал работает как остеокондуктор с дополнительной остеоиндуктивной активностью за счет связывания костных морфогенетических белков (КМБ) и образования депо природных стимулирующих факторов роста.
Другими перспективными продуктами является так называемая холодная биокерамика и препараты на ее основе, которые содержат альгинат натрия, гидроксиапатит, трикальцийфосфат и биомолекулы.
Материалы стимулируют рост и дифференциацию клеток костной структуры, вместе с тромбоцитарной мембраной из аутологичной плазмы они выполняют функцию раздельно-защитной мембраны и отличаются высокими остеоиндуктивными свойствами за счет факторов роста.
Высокую клиническую эффективность демонстрируют «Остеоматрикс» и «Биоматрикс», которые являются формами гидроксилапатита. Материалы имеют высокую для своего класса биологическую совместимость и не вызывают иммунной реакции в организме реципиента.
При всех положительных качествах препаратов на основе гидроксиапатита есть данные о том, что после заполнения дефектов гранулами на их основе происходит инкапсуляция гранул грубоволокнистой тканью.
Melcher (1976) и Stahe (1997) опытным путем установили, что пародонтальные ткани, которые располагаются на грани послеоперационного пародонтального дефекта, имеют разную скорость регенерации.
Быстрее регенерирует эпителий, который, выстилая дефект, препятствует регенерации цемента, периодонта и костной ткани.
Эти исследования стали обоснованием для разработки метода направленной тканевой регенерации и создания мембраны-барьера.
Первоначально применялась мембрана Millipore Filter, которую делали из ацетатцелюлозы. Она, как и мембраны Gore-Tex и TefGen, не резорбировалась, что в клинических условиях проявлялось рядом недостатков:
-
Необходимость повторной операции для удаления мембраны.
-
Отсутствие формирования надкостницы и ангиогенеза.
-
Потенциальная возможность инфицирования.
В связи с этим ученые разработали мембраны, способные биорезорбироваться (поликарбонатные, коллагеновые, композитные, политетрафлорэтиленовые, из силиконовой резины, поликапролактоновые).
Основным преимуществом таких мембран является образование высококачественного клеточного соединения между тканями корня и тканями десны и отсутствие необходимости повторного оперативного вмешательства.
Положительно зарекомендовало себя использование в качестве резорбируемой мембраны консервированной твердой оболочки головного мозга, которая имеет слабую иммуноспецифичность и высокую репаративную способность, стимулирует процессы восстановления и трофики тканей.
Но некоторые авторы считают, что использование мембран препятствует сцеплению десневого лоскута с поверхностью обнаженных корней зубов, прорастанию эпителия и созданию условий для регенерации тканей, образующих периодонтальную связку.
Это объясняется тем, что только периодонтальные ткани способны трансформироваться в цементобласты и блокировать клеточный рост других тканей, обеспечивая этим формирование нового зубодесневого соединения.
Вызывают интерес остеопластические материалы для пародонтологии, содержащие чистую фазу β-трикальцийфосфата. Они обеспечивают полную биологическую резорбцию и активируют репаративную регенерацию кости.
При этом формирование новой кости происходит параллельно с процессом резорбции и отпадает необходимость в применении сдерживающих мембран.
Полная резорбция β-трикальцийфосфата и одновременное замещение дефекта новой костью происходит за несколько месяцев. Следовательно, остекондуктивные свойства ярко выражены.
В эксперименте установлено, что это сопровождается снижением удельной площади имплантированных частиц, повышением индекса остеоинтеграции и удельной плотности трабекул в реактивной зоне.
Материалы на основе ТКФ могут быть синтетическими, поэтому они исключают риск передачи белков, прионов и других чужеродных агентов.
Пористость ТКФ обусловливает формирование остеона зрелой костной ткани на поверхности гранул. Кроме того материал является рентгенконтрастным, что позволяет осуществлять динамические клинические наблюдения за его поведением в организме реципиента.
Использование таких остеопластических материалов при хирургическом лечении генерализованного пародонтита с остеопенией способствует более благоприятной динамике рентгенологических показателей.
Недавно в стоматологической практике был применен способ «тоннельной реваскуляризации», который используют при хирургическом лечении ГП.
При этом создают поднадкостничные перфорационные отверстия и формируют поднадкостничные «тоннели» для улучшения репаративных процессов в области альвеолярного отростка, исключая травму костной ткани, которая возникает при компактостеотомии.
Перфорационные отверстия являются «тоннелями» для прорастания кровеносных сосудов под надкостницу, создавая условия реваскуляризации тканей пародонта, улучшая трофические и репаративные процессы в ткани.
Заключение
Таким образом, использование мощного арсенала различных стимуляторов репаративного остеогенеза позволяет достичь регенерации кости альвеолярного отростка, а процесс регенерации протекает без промежуточной реконструкции и его атрофии, в отличие от рутинного процесса заживления.
Каждый из методов и материалов имеет свои преимущества и недостатки.
Это связано с разными остеогенными качествами, наличием токсических свойств (формалинизированные материалы), антигенностью (костный мозг), сложностью заготовки и приготовления материала (брефоматериал), отсутствием антимикробных свойств и так далее.
Современная пародонтальная хирургия вооружена значительным арсеналом хирургических методик и материалов различной природы.
Несмотря на постоянное совершенствование операционных технологий с помощью модификаций и дополнений, еще не всегда удается эффективно приостановить патологический процесс в пародонте.
Это обуславливает необходимость разработки инновационных способов хирургического лечения генерализованного пародонтита.