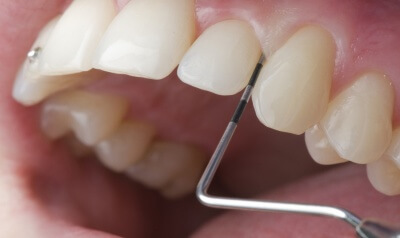
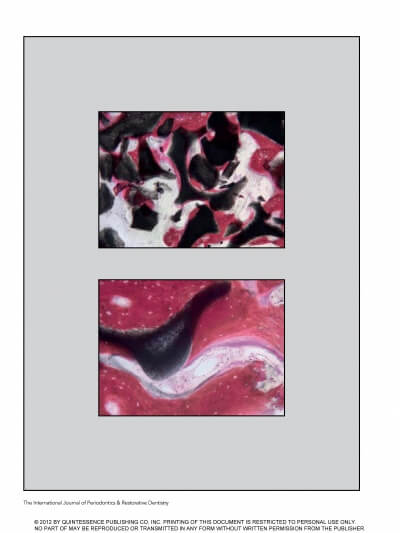
Костные блоки для стоматологии: биологические и физические свойства
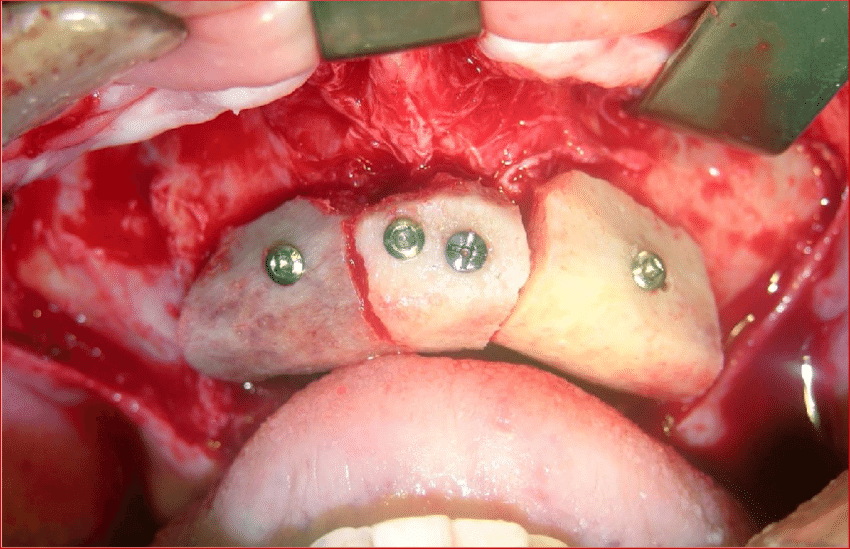
Атрофия альвеолярного отростка верхней челюсти — нежелательный процесс, который наблюдается после экстракции зуба. Было предложено множество вариантов лечения для улучшения результатов дентальной имплантации при данном сценарии.
Целью статьи является оценка биологических и физических свойств костных блоков из различных биоматериалов при атрофии альвеолярного отростка верхней челюсти.
Для этого проанализированы многочисленные зарубежные клинические данные, относящиеся к использованию этих биоматериалов.
Аутокость, аллогенные и ксеногенные костные блоки
После удаления зуба ремоделирование, ведущее к резорбции кости, считается обычным явлением. Резорбция гребня обусловила высокую популярность остеопластики в дентальной имплантации. Эта процедура направлена на восстановление ширины и высоты альвеолярного отростка для правильного размещения имплантата.
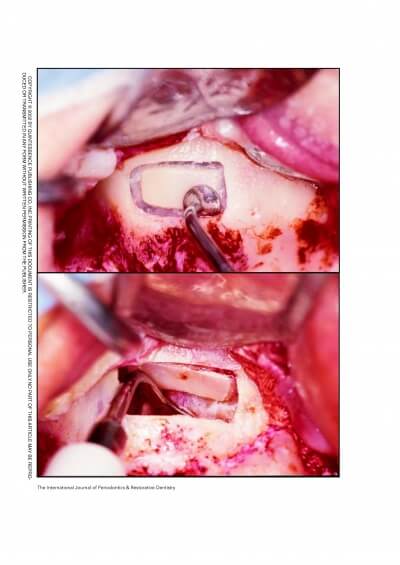
Были предложены многочисленные альтернативы, такие как дистракционный остеогенез и направленная регенерация кости с использованием костных материалов в виде частиц. Тем не менее, для обширных дефектов и сильно атрофированного альвеолярного отростка остеопластика костными блоками считается наиболее предсказуемой.
Аутогенная кость остается золотым стандартом для восстановления объема костной ткани. Аутокость получают из различных участков тела пациента, в зависимости от назначения.
Хотя внутриротовые костные аутотрансплантаты (нижнечелюстная ветвь, подбородочный симфиз) возможно получить менее травматично, количество материала часто оказывается недостаточным для выполнения процедуры.
Внеротовые костные аутотрансплантаты (гребень подвздошной кости) отвечают требованиям в отношении количества, зато они существенно увеличивают стоимость и ведут к некоторым нежелательным последствиям со сторны донорского участка.
Независимо от места забора материала, аутогенные костные блоки могут быть дополнительно классифицированы в зависимости от происхождения.
Например, внутримембранные костные трансплантаты (нижнечелюстная ветвь и кость голени) отличаются меньшей резорбцией кости. Процессы ремоделирования кости или «ползучей замены» занимают относительно больше времени по сравнению с эндохондральной костью (гребнем подвздошной кости).
Важно принимать это во внимание при планировании имплантологического лечения, чтобы материал не вызывал обширного ремоделирования кости, которое угрожает окончательному адекватному расположению дентального имплантата.
Аутологичная кость обладает остеогенными свойствами. Другими словами, кость способна потенциально разрастаться между границей трансплантата и костью хозяина. Тем не менее, недостатки, связанные с этим подходом, побуждают клиницистов использовать альтернативы, такие как аллогенные или ксеногенные костные блоки.
Альтернативные стратегии не только снимают проблему осложнений при заборе аутокости, но и сокращают время лечения, тем самым повышая удовлетворенность пациентов.
Механизм образования новой минерализованной ткани опосредован мезенхимальными клетками, которые дифференцируются в остеобласты и координируются при помощи гликопротеинов (морфогенетических белков кости).
После воспалительного процесса, который заканчивается постепенным замещением, образуется полноценная кость. Применительно к дентальной имплантации, это твердые ткани, обеспечивающие стабильность имплантата с дальнейшей остеоинтеграцией.
Аллогенные и ксеногенные костные блоки не содержат остеопрогениторных клеток. Следовательно, интеграция с нативной костью может быть затруднена.
Несмотря на данный факт, в литературе были продемонстрированы обнадеживающие результаты при использовании этих блочных трансплантатов для регенерации кости.
Что касается их происхождения, костные блоки могут быть получены от человека (аллотрансплантаты), или от животного, которые называются ксенотрансплантатами.
После забора трансплантаты должны быть тщательно обработаны и сохранены. Каждая компания-производитель разработала свой собственный процесс, который потенциально способен определять характеристики фирменного биоматериала.
Мы постараемся рассмотреть биологические и физические свойства блочных трансплантатов и биоматериалов, доступных для регенерации кости при атрофии альвеолярного отростка.
Свойства костных блоков из различных биоматериалов
Биоматериалом называют любой материл, который был разработан для взаимодействия с биологической системой, выступая в качестве основы для замены и регенерации, в данном случае, утраченной кости. К нему предъявляется ряд специфических требований.
Во-первых, биоматериал должен быть биосовместимым, то есть не должен идентифицироваться организмом хозяином как инородное тело и вызывать ответ.
Во-вторых, биоматериал должен обладать достаточной механической прочностью и долговечностью для выполнения задачи, ради которой он разработан.
Кроме того, он должен быть химически стабильным (не проявлять токсических или канцерогенных свойств, учитывая длительное пребывание в организме).
Для блочных трансплантатов, используемых в стоматологии, идеальный биоматериал с клеточной и молекулярной точек зрения должен обладать следующими свойствами:
- Структура, которая позволяет остеогенным клеткам достигать всего пространства блока путем остеокондукции и остеоиндукции. Чтобы обеспечить рост остеобластов и образование минерализованной ткани, размер микропор должен составлять порядка 180–600 мкм. Это имеет решающее значение, поскольку остеобласты (15–50 мкм) и стволовые клетки (5–12 мкм) должны беспрепятственно проникать в блок.
- Скорость деградации биоматериала должна соответствовать процессу ремоделирования, поскольку костный блок будет в конечном замещен новообразованной тканью.
- Трабекулоподобные структуры, которые образуют каркас, должны оставлять достаточно места для образования кровеносных сосудов эндотелиальными клетками. Сосуды будут поставлять все питательные вещества и костные клетки в этот каркас.
Когда это происходит в аутогенном костном блоке, биоматериалы проходят три этапа: (1) колонизация клетками хозяина; (2) деградация биоматериала в ходе ремоделирования; (3) созревание новообразованной кости и интеграция с костью реципиентного участка.
Биоматериалы для остеопластики должны обладать и рядом дополнительных свойств, кроме биологических. Это позволит костному блоку взаимодействовать с микроокружением тканей хозяина, повысит вероятность образования кости и долговременную стабильность:
- Механические свойства: упругость, жесткость, хрупкость, прочность, пластичность. Результат сочетания этих механических свойств будет определять возможность применения материала в качестве основы для регенерации кости. Однако важно отметить, что, чем жестче биоматериал, тем дольше он резорбируется.
- Поверхностные явления: важно принимать во внимание внутреннюю энергию, поверхностное натяжение, смачиваемость, а также адгезию и когезию биоматериала, который будет использоваться для регенерации кости. Эти свойства отвечают за агрегацию и прикрепление жизненно важных остеогенных клеток к каркасу.
- Физические свойства. В эту группу входят три основных свойства: термические (тепловое расширение, тепловое сжатие, теплоизоляция, температура плавления), электрические (электропроводность, удельное электрическое сопротивление, оральный гальванизм) и оптические свойства (цвет, эстетика).
- Химические свойства: учитывается токсичность, химическая стабильность, период полураспада, воспламеняемость или энтальпия образования.
- Реологические свойства: кажущаяся вязкость, коэффициенты нормальной силы, модуль накопления, комплексная вязкость и комплексные функции нелинейной вязкоупругости.
Роль васкуляризации в остеопластике
Биоматериалы, используемые в регенерации костной ткани, лишены клеток, белков и сосудов. Таким образом, риск передачи заболевания сводится к минимуму.
Клетки реципиентного участка трансплантата должны осуществлять процесс неоангиогенеза, что является важным этапом успешной регенерации.
Неоваскуляризация действительно имеет фундаментальное значение, поскольку она обеспечивает снабжение бессосудистых каркасов кислородом и питательными веществами, необходимыми для роста и дифференцировки клеток. Соответственно образование кости и рассасывание блок-трансплантата зависят от процесса неоангиогенеза.
В процесс неоангиогенеза вовлечены многочисленные факторы роста:
- фактор роста фибробластов (FGF)
- фактор роста эндотелия сосудов (VEGF)
- некоторые подгруппы трансформирующих факторов роста бета (TGF-β)
- транскрипционный фактор, индуцирующий гипоксию (HIF)
- фактор роста гепатоцитов (HGF)
- тромбоцитарный фактор роста (PDGF-BB)
- инсулиноподобный фактор роста (IGF-1, IGF-2)
- нейротрофический фактор роста (NGF)
- ангиопоэтин (Ang-1)
VEGF и его рецепторы отвечают за молекулярный и клеточный каскад, обеспечивающий развитие эндотелиальной системы посредством васкулогенеза, ангиогенеза и образования лимфатической сети. Фактор роста эндотелия сосудов играет важную роль в развитии скелета, а также в восстановлении и регенерации кости.
FGF отвечает за стимулирование пролиферации и дифференцировки эндотелиальных клеток и фибробластов. TGF активизирует развитие внеклеточного матрикса. HIF опосредует влияние гипоксии на клетки. Ангиопоэтин стабилизирует кровеносные сосуды.
Кроме того, фактор роста гепатоцитов действует на эпителиальные и эндотелиальные клетки, способствуя нормальной регенерации органов и заживлению ран. Традиционно применяемые в качестве экзогенных факторов роста при регенерации кости, представители многочисленного семейства PDGF играют важную роль в ангиогенезе.
IGF, в свою очередь, оказывает воздействие на эндокринные механизмы реципиента. Наконец, нейротрофические факторы роста (нейротрофины) отвечают за рост нервных клеток внутри новообразованной костной ткани.
При остеопластике с использованием блочных трансплантатов в качестве каркаса возникают новые тенденции, поскольку, в отличие от аутогенных трансплантатов, ранний неоангиогенез необходим для выживания и интеграции биоматериала.
Такие методы, как доставка стволовых клеток и факторов роста для ускорения процесса, были недавно испытаны с получением многообещающих клинических результатов. Однако нам все еще не хватает научных данных, чтобы сделать какое-либо убедительное утверждение по поводу их использования.
Разновидности костных блоков для стоматологии
Существенные недостатки аутогенной кости, такие как осложнения после забора материала, стоимость и чрезмерная резорбция побудили клиницистов искать альтернативные опции.
Аллогенные костные блоки
Использование аллотрансплантатов представляет собой отличную альтернативу аутокости, поскольку костные блоки получают от тех же биологических видов, что и реципиент.
Первые костные аллотрансплантаты были применены в конце XIX века группой хирургов, которые восстановили зараженную плечевую кость с помощью трансплантата, извлеченного из большеберцовой кости того же пациента.
Создание в 1990 году Военно-морского банка тканей США стало значительным движущим фактором, влияющим на использование костных аллотрансплантатов. С тех пор изучение и клиническое использование этого материала за рубежом активизировалось.
Свойства аллотрансплантата
Свойства аллотрансплантата напрямую связаны с его обработкой. Аллогенные блочные трансплантаты могут быть свежие, замороженные и лиофилизированные.
В настоящее время подавляющее большинство трансплантатов тщательно проверяется, обрабатывается, хранится и распространяется в соответствии с жесткими национальными и международными стандартами. В Соединенных Штатах, например, эти процессы регулируются Американской ассоциацией банков тканей.
Риск передачи заболевания сводится к минимуму с помощью вышеуказанных процессов. Кроме того, во время подготовки трансплантата антигенные компоненты тщательно удаляются, чтобы предотвратить потенциальный иммунный ответ реципиента.
Свежие и замороженные аллогенные костные блоки сохраняют свои остеоиндуктивные и остеокондуктивные свойства. Это обеспечивает более быстрое ремоделирование костной ткани по сравнению с использованием лиофилизированных аллотрансплантатов.
Тем не менее, риск передачи инфекционного заболевания и реакции реципиента несколько повышен, тогда как реакция на лиофилизированные аллотрансплантаты минимальна.
Этот факт объясняется элиминацией любых клеток путем двукратной промывки костного блока антибиотиком в течение 1 часа, с последующим хранением при температуре -70°С.
Другая проблема заключается в том, что из-за сушки механические свойства ухудшаются. Следовательно, может произойти микроразрушение трансплантата.
Для аллогенных костных блоков перед имплантацией нужна регидратация, чтобы восстановить некоторые механические свойства.
Компания Zimmer Biomet Dental (Карлсбад, Калифорния) запатентовала подходящую технологию. Это процесс Tutoplast, который предусматривает очистку и ультразвуковую липидизацию в ацетоне, осмотическую и окислительную обработку, заканчивающуюся дегидратацией в ацетоновых ваннах и стерилизацию гамма-излучением.
Преимуществом этого технологического процесса является более высокая сохранность минералов и коллагенового матрикса, а также более быстрое ремоделирование.
Клинические результаты
Аллогенные блочные трансплантаты являют собой относительно новую альтернативу аутокости для горизонтальной и / или вертикальной аугментации альвеолярного отростка верхней челюсти. В 1999 году был зарегистрирован первый случай использования аллогенного костного блока в стоматологии с этой целью.
В этом случае дентальные имплантаты для оральной реабилитации успешно установили через три месяца после процедуры трансплантации. С тех пор было опубликовано множество проспективных клинических испытаний на людях, подтвердивших целесообразность использования этой разновидности биоматериалов у человека.
Судя по клиническому опыту, воздействие негативных факторов полости рта на аллотрансплантат часто приводит к негативным результатам лечения.
Кроме того, аллогенные костные блоки гораздо хуже показывают себя в нижней челюсти, чем в верхней челюсти. Это может объясняться трудностями при формировании лоскута и более тонким биотипом мягких тканей данной области.
В процессе заживления происходит резорбция аллогенного костного трансплантата, аналогично аутогенной кости. Через шесть месяцев после процедуры наблюдается большая потеря костной массы сравнению с аутогенной костью из нижней челюсти (52,00 ± 25,87% против 25,00 ± 12,73% соответственно).
Недавний систематический обзор показал, что применение аллогенных костных блоков для горизонтальной аугментации альвеолярного отростка верхней челюсти имеет великолепные клинические перспективы.
Были достигнуты не только высокие показатели выживаемости трансплантата и имплантата (98,0% и 96,9% соответственно), но также увеличение кости в горизонтальной плоскости на 4,79 мм за средний период наблюдения 23,9 месяца.
Ксеногенные костные блоки
Ксенотрансплантаты, полученные из генетически отличающихся видов, представляют собой другую перспективную альтернативу аутогенным блочным трансплантатам. Подобно человеческим аллотрансплантатам, отсутствие остеогенных свойств делает их менее предсказуемыми с точки зрения интеграции в кость реципиента.
Отсутствие человеческих остеогенных клеток превращает ксеногенные костные блоки в безжизненные каркасы, лишенные остеоиндуктивного потенциала.
Несмотря на новизну использования в качестве блочных трансплантатов для аугментации сильно атрофированной кости, этот биоматериал широко используется в качестве костного трансплантата в виде макрочастиц, демонстрируя отличные результаты благодаря поддержанию объема и стабильности.
До настоящего времени в мире недостаточно научных данных относительно ксеногенных костных блоков. Известно, что васкуляризация этого биоматериала является критичной для успеха, и, следовательно, при трехстеночных дефектах он более надежный.
Однако преимущество использования ксеногенного биоматериала состоит в том, что благодаря низкой скорости резорбции пространство сохраняется на протяжении более длительного периода времени.
В настоящее время доступны два типа ксеногенных костных блоков для аугментации альвеолярного отростка: бычий и лошадиный.
Хотя депротеинизированная бычья кость хорошо изучена и надежна, конскую кость в последнее время называют менее хрупкой и более функциональной.
Однако необходимы дополнительные исследования для проверки жизнеспособности этого варианта по сравнению с аутогенными и аллогенными костными блоками.
Свойства ксенотрансплантата
В отличие от человеческой кости, ксеногенные трансплантаты не имеют остеоиндуктивного потенциала. Поэтому их применяют только в качестве каркаса для поддержания пространства и обеспечения миграции клеток-предшественников.
Утверждается, что ксеногенные биоматериалы, хотя и не обладают остеоиндуктивным потенциалом, служат каркасом с медленным рассасыванием, способным стимулировать формирование кости.
Широко известным в России и республиках СНГ продуктом данной серии являются ксеногенные костные блоки для стоматологии и травматологии Остеоматрикс (ООО «Конектбиофарм», город Москва).
Этот биоматериал бычьего происхождения не содержит иммуногенных органических веществ, поэтому хорошо переносится пациентами. По качеству, функциональности и безопасности Остеоматрикс не уступает европейским и американским аналогам, одновременно будучи доступным и экономически выгодным вариантом.
Исследования, проведенные в России и за рубежом, демонстрируют многообещающие результаты использования Остеоматрикс в стоматологии и челюстно-лицевой хирургии.
Клинические результаты
Как мы уже говорили, объем научных данных о применении ксеногенных костных блоков остается ограниченным. На данный момент в мире было проведено не более десяти крупных исследований, посвященных применению этого биоматериала в стоматологии.
Ксеногенный блок-трансплантат рекомендован для аугментации альвеолярного отростка. Steigmann и коллеги представили первый отчет о случае, когда этот биоматериал успешно использовался для горизонтальной аугментации в области верхней челюсти.
Что касается резорбции, исследование Araújo на собаках показало, что костные блоки Geistlich Bio-Oss сохраняют размеры при умеренном количестве новой кости, сформированной у основания трансплантата, в то время как аутогенные блочные трансплантаты претерпевают резорбцию на уровне 30% и 50%.
De Santis и коллеги в исследовании на собаках продемонстрировали высокую объемную стабильность депротеинизированной бычьей кости по сравнению с аутогенными костными блоками из нижней челюсти (резорбция 0,2 мм против 0,9 мм соответственно).
Заключение
Аллогенные и ксеногенные костные блоки в стоматологической практике составляют достойную конкуренцию аутогенной кости для аугментации альвеолярного отростка.
Тем не менее, доказательства, подтверждающие преимущества ксеногенных блочных трансплантатов, остаются минимальными; необходимы длительные исследования.
Кроме того, использование композитных биоматериалов, пропитанных факторами роста, представляет интересную область для дальнейшего изучения.