Ксеноматериалы для костной пластики: краткий обзор исследований

Мы решили проанализировать публикации по современным костным трансплантатам, существующим и перспективным методам их использования; обобщили характеристики, преимущества и ограничения ксеноматериалов для костной пластики.
Сегодня существуют сотни разновидностей костных трансплантатов для регенерации костей, включая аутотрансплантаты из организма пациента и ксеноматериалы, производимые из других биологических видов. До последнего времени аутотрансплантаты оставались золотым стандартом для этой цели, так как содержат остеогенные клетки, остеоиндуктивные факторы роста и остеокондуктивные каркасы, которые необходимы для формирования новой кости.
Однако применение аутотрансплантатов в клинической практике ограничено из-за дополнительной травматизации и высокого риска осложнений. Однако при несовершенной технологии обработки аллографты и ксеноматериалы для костной пластики несут риск передачи инфекционных заболеваний и отторжения.
Тканевая инженерия является новым и развивающимся направлением, которое призвано нивелировать недостатки нынешних материалов для костной пластики и улучшить процессы заживления переломов и дефектов кости.
Комбинированное использование внеклеточного матрикса, ростовых факторов, дополненное генной терапией и развивающейся в последние годы 3D-печатью, открывает новые перспективы для стоматологии и ортопедической хирургии.
Общие характеристики материалов для костной пластики
В отличие от остальных тканей, кость способна полностью регенерировать: во многих случаях повреждения и переломы заживают без образования рубцов. Тем не менее, при патологических переломах или крупных дефектах костной ткани естественные процессы восстановления оказываются недостаточными.
Нарушенное кровоснабжение, инфекция кости или окружающих тканей, а также системные заболевания могут отрицательно влиять на заживление, что приводит к задержке срастания.
По статистике, кость является второй наиболее часто пересаженной тканью после крови.
Костный трансплантат — материал, который способствует заживлению кости отдельно или в комбинации с другими материалами посредством остеогенеза, остеоиндукции и остеокондукции.
Выбор идеального материала для костной пластики зависит от нескольких факторов, таких как жизнеспособность ткани, размер дефекта, размер трансплантата, форма и объем, биомеханические характеристики, обработка трансплантата, стоимость, этические проблемы, биологические характеристики и связанные с ними осложнения.
Материалы, используемые в костной пластике, можно разделить на несколько основных категорий: аутотрансплантаты, аллотрансплантаты и ксенотрансплантаты.
Каждый имеет свои преимущества и недостатки. Аллографты и ксенографты отличает наличие остеоиндуктивных и остеокондуктивных свойств, но они не обладают остеогенными свойствами аутокости.
Будучи золотым стандартом при восстановлении мелких дефектов кости, аутотрансплантаты обладают выраженными остеогенными свойствами, то есть высоким потенциалом заживления, моделирования и ремоделирования костной ткани.
Боль в донорском участке, а также связанные с хирургической операцией риски, такие как повреждение кровеносных сосудов или внутренних органов, являются одними из основных недостатков аутокости.
По этим причинам в разное время было предложено и опробовано несколько альтернативных материалов для костной пластики. Аллотрансплантаты являются наиболее очевидным выбором, однако с этими материалами возникает проблема передачи инфекций, отказа пациентов по морально-этическим соображениям, а также высокая стоимость.
Аллографты гораздо хуже аутокости интегрируются в ткани реципиента.
Ксенографты, помимо недостатков аллотрансплантатов, несут в себе риски передачи зоонозных заболеваний, а отторжение трансплантата является более вероятным при условии недостаточно эффективной обработки сырья.
Отметим, что эти недостатки удалось нивелировать благодаря инновационной очистке и стерилизации продукции (как например, высокоэффективная радиационная стерилизация при производстве продукции Остеоматрикс). Сегодня клиника может купить ксенографт для костной пластики, не сомневаясь в высоком качестве и безопасности для пациентов.
Несмотря на совершенствование технологии производства ксенографтов, за рубежом интенсивно развивается альтернативное направление — тканевая инженерия. Используя методы тканевой инженерии, исследователи надеются создавать новые каркасы и тканевые трансплантаты с целью избавиться от недостатков традиционных материалов и улучшить их свойства: остеогенность, остеокондуктивность и остеоиндуктивность.
Тканевая инженерия имеет ограничения, в том числе использование большого количества дорогостоящих и сложных материалов для производства биоинженерных костных трансплантатов или каркасов. Трансляционные исследования по каждому компоненту оказываются ограниченными, что требует времени и затрат на внедрение.
Эксперты признают: некоторые важные аспекты взаимодействия трансплантат-хозяин и иммунного ответа на биоинженерные костные трансплантаты до сих пор не изучены.
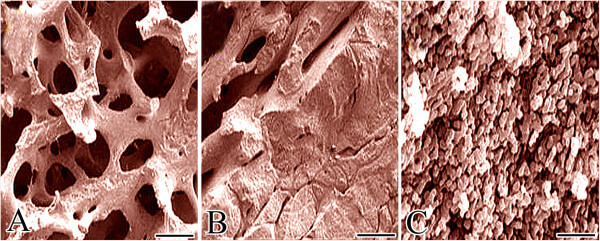
Микрофотографии природных материалов для костной пластики. A: Трабекулярный или губчатый костный трансплантат. B: Кортико-губчатый костный трансплантат. С: Кортикальный или компактный костный трансплантат.
Структура костных трансплантатов
Костные трансплантаты могут быть кортикальными, губчатыми и кортикально-губчатыми.
Кортикальная кость имеет более высокое содержание минералов, чем трабекулярная или губчатая кость. Кроме того, учитывая наличие пор достаточного размера в структуре губчатой кости, последняя является более остеогенной, чем кортикальная.
Прочность на сжатие у кортикальной кости выше, чем у губчатой. При выборе материала для костной пластики или комбинации хирург должен учитывать эти фундаментальные различия в структуре. Кортикальные костные трансплантаты используются в основном для структурной поддержки и повышения прочности, а губчатые — для остеогенеза.
Структурная поддержка и остеогенез могут сочетаться, что является одним из наиболее важных преимуществ использования кортико-губчатой кости. Трабекулярная кость обычно применяется при несращенных переломах, дефектах челюстно-лицевой области, позвоночника.
Такие костно-пластические материалы не имеют значительной механической прочности, однако просты в использовании. Пористая структура губчатых костных трансплантатов может усиливать интеграцию, обеспечивая более быструю реваскуляризацию.
Кортикальная кость применяется реже, и ее можно использовать в качестве накладных трансплантатов. Накладной костный трансплантат может потребоваться для увеличения атрофированной кости за пределами анатомических границ скелета.
Примером является трансплантат, который применяют для увеличения ширины атрофированной альвеолярной кости будущего участка имплантации. Правильное позиционирование трансплантата играет главную роль в процессе заживления и, следовательно, в успехе лечения.
Когда трансплантат используется для заполнения костного дефекта в пределах анатомического скелета, термин вкладной трансплантат является наиболее подходящим.
Скорость резорбции накладных трансплантатов выше, чем у вкладных, по двум причинам.
Во-первых, накладные трансплантаты менее подвержены влиянию сосудистой сети реципиента, что приводит к снижению ремоделирования кости. Во-вторых, накладные трансплантаты всегда испытывают на себе давление окружающих мягких тканей, что приводит к большей остеокластической резорбции на участках с наибольшим давлением.
Ключевые свойства костных трансплантатов
Прежде чем купить ксенографт для костной пластики или другой продукт, необходимо понимание биологических свойств и потенциальной пользы того или иного материала для пациента. Идеальный костно-пластический материал должен обладать остеогенными, остеокондуктивными, остеоиндуктивными и остеоинтегративными свойствами.
Остеогенность — способность образовывать кость путем дифференцировки остеопрогениторных клеток, которые либо присутствуют в кости реципиента, либо поступают из трансплантата. Данное свойство в основном присуще аутокости, в отличие от аллографта или ксенографта, поскольку клеточные структуры последних имеют низкую жизнеспособность.
Остеоиндуктивность — это способность трансплантата индуцировать дифференцировку мультипотентных мезенхимальных стволовых клеток из окружающих тканей реципиента с образованием остеопрогениторных клеток и развитием остеобластов.
Данное свойство было обнаружено у факторов роста, включая костные морфогенетические белки (BMP). Среди них BMP-2 и BMP-7, трансформирующий фактор роста бета (TGF-β), фактор роста фибробластов, инсулиноподобный (IGF) и тромбоцитарный фактор роста (PDGF).
Остеокондуктивность определяет способность трансплантата действовать как рассасывающийся каркас, механически поддерживающий врастание сосудов и новой кости от границ дефекта.
Наконец, необходима остеоинтеграция — это связывание с окружающей костью без промежуточного слоя фиброзной ткани, что позволяет внедриться в ткань хозяина.
Все материалы для костной пластики могут быть описаны этими четырьмя свойствами.
Среди всех типов костных трансплантатов только аутокость обладает всеми вышеуказанными свойствами. Аллографты и ксенографты демонстрируют только два или 3 из 4 признаков идеального костно-пластического материала — это остеоинтеграция, остеокондукция и, возможно, остеоиндукция, но не имеют остеогенных свойств
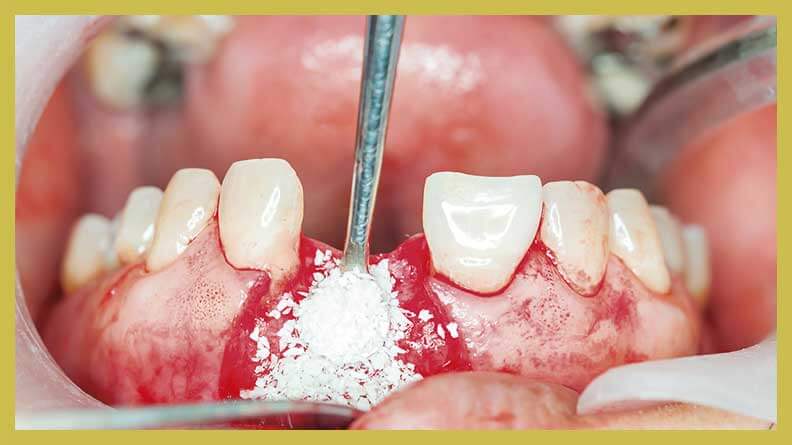
Новый опыт применения ксеноматериалов для костной пластики
Альтернативой аутогенным костным трансплантатам являются ксеноматериалы, также известные как гетерологичные или ксеногенные трансплантаты. Эти костно-пластические материалы берут от представителей другого биологического вида (например, бычья или свиная кость), которая подвергается деминерализации, депротеинизации и лиофилизации.
Впервые бычья кость была внедрена Маатцем и Бауэрмайстером в 1957 году.
Обычно они предлагаются только в виде кальцинированного матрикса.
Кораллы madrepore и / или millepore собирают и обрабатывают, чтобы они превратились в «гранулы кораллового происхождения» (CDG) или другие продукты. Ксенотрансплантаты на основе кораллов в основном представляют собой карбонат кальция (со значительным содержанием фторидов, полезных в контексте трансплантации для стимулирования развития костей), в то время как кость человека состоит из гидроксиапатита (ГАП) с карбонатом и фосфатом кальция.
Коралловый материал либо промышленно превращают в гидроксиапатит посредством гидротермального процесса, либо этот просто процесс пропускается, и ксенографт остается в изначальном состоянии для обеспечения лучшей резорбции. Затем коралловый продукт насыщается гелями и растворами, улучшающими рост ткани.
В январе 2010 года итальянские ученые заявили о прорыве в использовании древесины в качестве костно-пластического материала, хотя этот метод не был воплощен в жизнь до самого 2015 года.
Различные виды дерева подвергаются пиролизу в инертной атмосфере, углеродистый остаток насыщается солями кальция и, наконец, нагревается до высокой температуры с целью получения высокопористого кристаллизованного материала. Последний отличается более высокой пористостью, чем трабекулярный титан и пористые керамические продукты.
Авторы утверждают, что костно-пластический материал на основе древесины обеспечивает лучшую интеграцию во время роста кости и будет больше сгибаться, чем металлические или твердые керамические трансплантаты.
Ксеноматериалы для костной пластики (Остеоматрикс, Биоматрикс) дают великолепные в стоматологии, а также продолжают активно исследоваться в ортопедической хирургии.
Очевидным преимуществом их является теоретически неограниченный источник сырья.
Основная проблема, связанная с продуктами, полученными из крупного рогатого скота — потенциальная передача зоонозных заболеваний и прионных инфекций, таких как губчатый энцефалит крупного рогатого скота (губкообразная энцефалопатия, BSE).
Ксенографты, подобно аллографтам, теряют остеогенные и частично остеоиндуктивные свойства во время агрессивной обработки. В прошлом животные продукты действительно не славились эффективностью, однако современные технологии обеспечивают высокую безопасность и отличный клинический результат в стоматологии.
Keskin и соавторы оценивали эффективность аутологичного костного мозга при лечении дефектов локтевой кости, заполненных ксенографта бычьего происхождения у кроликов. Костный дефект в локтевых суставах был произведен путем удаления 1-сантиметрового сегмента.
Лечение дефекта выполнялось одновременно с использованием ксенографта бычьего происхождения, комбинации ксенотрансплантата и костного мозга или, на пятый день после заполнения сегмента, ксеногенным материалов и аутокостью.
Авторы пришли к выводу, что, когда ксенографты сочетались с аутогенным красным костным мозгом, ключевые недостатки материала удается полностью компенсировать.
Кроме того, они заключили, что губчатый ксенотрансплантат может обеспечить подходящую среду для остеогенеза клетками костного мозга.
Ряд других исследователей (Emami M., Oryan A.) считают, что клетки костного мозга обеспечивают лучшие результаты при заживлении кости, без значительных осложнений.
Athanasiou и соавторы изучали ксеноматериал производства Греции, представляющий собой очищенный матрикс трабекулярной кости, который преимущественно содержит коллаген I типа и гидроксиапатит. Для этого они проделывали отверстия диаметром 4,5 мм в латеральном мыщелке бедра обеих лап у 90 кроликов, выделенных в шесть экспериментальных групп.
Дефекты заполнялись различными материалами, включая аутокость, аллогенный деминерализованный костный матрикс, очищенный матрикс бычьей губчатой кости, заменитель гидроксиапатита французского производства и сульфат кальция. Шестая группа — контрольная.
Животных умерщвляли через 1, 3 и 6 месяцев после процедуры имплантации, после чего образцы ткани подвергались гистологическому исследованию. Самые высокие гистологические оценки были получены с использованием аутотрансплантата губчатой кости. Бычий ксенографт был вторым лучшим по гистологической шкале, остальные же материалы дали похожие результаты, но значительно уступали ксеноматериалу и аутокости.
В 2013 году Bigham-Sadekh и соавторы провели исследование с применением фетального бычьего деминерализованного костного матрикса, сравнивая новый материал с кортикальной аутокостью и порошком ксеногенного хряща крупного рогатого скота.
При лечении костных дефектов у собак фетальный бычий деминерализованный костный матрикс превосходил все материалы, кроме кортикальной аутокости — последняя вновь оказалась наиболее эффективность за счет остеогенных свойств.
Тем не менее, в практике доступность, отсутствие морально-этических проблем, наличие остеокондуктивных и остеоиндуктивных свойств ксеноматериала для костной пластики зачастую делают его предпочтительней аутокости.