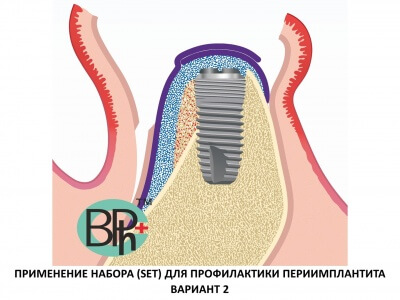
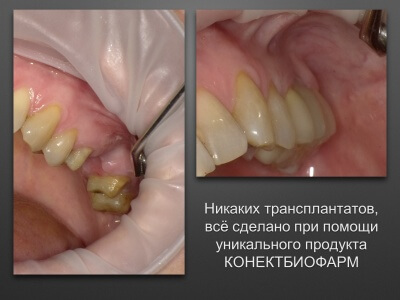
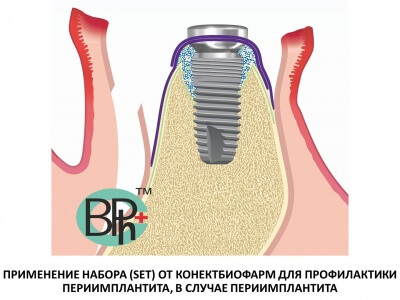
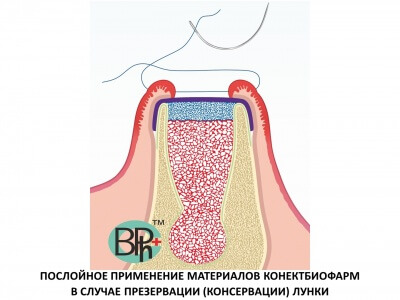
Увеличение альвеолярного отростка: нанотехнологии и новые материалы

Реконструкция и восстановление размеров альвеолярной кости — это сложная задача для стоматологии и челюстно-лицевой хирургии. Важнейшей целью терапии является преимущественно увеличение костной массы у пациентов, которые потеряли ткань в результате нескольких состояний, таких как пародонтоз, старение, остеопороз, неопластическая патология, врожденные пороки или травма.
В настоящее время аутотрансплантация из экстраорального или интраорального донорского участка признается «золотым стандартом» и пока является наиболее часто практикуемым подходом для увеличения альвеолярного отростка.
Критическими ограничениями этого традиционного подхода являются осложнения со стороны донорского участка, недостаточное кровоснабжение костного трансплантата, связанная с операцией боль и дискомфорт. По указанным причинам аутологичная трансплантация применяется в ограниченном количестве случаев.
Альтернативные источники костных материалов включают аллотрансплантаты (трансплантаты, происходящие от другого человека) и ксенотрансплантаты (трансплантаты, происходящие от разных видов, например, крупного рогатого скота или свиньи). Однако эти заменители также имеют некоторые недостатки, такие как возможность иммунного отторжения и передачи патогенов от донора к хозяину.
Еще одно направление разработки материалов для увеличения альвеолярного отростка — материалы из полимеров, керамики или металлов. Аллопластические материалы имеют ряд недостатков, таких как неоптимальная интеграция с нативной тканью в месте дефекта и потенциальную неудачу процедуры из-за усталости материала или инфекции, вызванной во время имплантации. В дополнение к этому, их использование ограничено в местах с повышенным механическим напряжением или нагрузкой.
Роль каркасов в тканевой инженерии и регенеративной медицине
Из-за недостатков и ограничений существующих костных материалов за последние несколько десятилетий появилось несколько новых подходов, включающих тканевую инженерию и регенеративную медицину (TE / RM).
Фундаментальная концепция, лежащая в основе TE / RM, заключается в использовании каркасов («скаффолдов») отдельно или в сочетании с фактором роста, доставкой клеток и / или генов с целью формирования конструкции, которая стимулирует ускоренное восстановление и / или регенерацию тканей.
Существует четыре решающих фактора, которые необходимо учитывать при TE / RM:
-
Клетки, которые представляют фундаментальную структурную единицу любой ткани.
-
Матрикс, представляющий собой «каркас», поддерживающий рост клеток с образованием в конечном итоге полностью организованная здоровой ткани.
-
Биологические факторы, такие как факторы роста (GF) и морфогенетические белки кости (BMP), которые направляют клеточную активность и формирование ткани.
-
Васкуляризация для обеспечения кислородом и питательными веществами для клеточного метаболизма, а также для удаления продуктов распада тканей.
Текущие ограничения в стратегиях тканевой инженерии и регенеративной медицины костей включают нарушение клеточной дифференцировки, неадекватный синтез внешних факторов, необходимых для эффективного остеогенеза, и, что наиболее важно, недостаточную механическую прочность и физико-химические свойства обычных каркасов.
Традиционно используемые «скаффолды» в комбинации с факторами роста или клетками не всегда обеспечивают успешную регенерацию кости в клинических условиях, как правило, из-за ограниченной способности контролировать деградацию каркаса, а также скорость высвобождения биологических факторов и лекарственных веществ.
В центре внимания настоящего обзора будет краткое введение в нано-каркасы, TE / RM и роль нанотехнологий и новых материалов для увеличения альвеолярного отростка.
Материал каркасов играет ключевую роль в регенерации тканей, поскольку он обеспечивает микросреду, подходящую для клеточной адгезии, пролиферации и дифференцировки.
Идеальный материал каркаса для восстановления костной ткани должен быть биосовместимым, должен иметь контролируемую деградацию и соответствующие физико-химические характеристики, чтобы моделировать структуру внеклеточного матрикса.
Он должен быть в состоянии уравновесить различные комбинации материалов с конкретными функциями при помощи специальной поверхности, инкапсуляции клеток или контролируемого высвобождения веществ. Кроме того, каркас должен инициировать и контролировать специфические события, происходящие на клеточном и тканевом уровне.
В тканевой инженерии на основе каркаса каркас должен выполнять несколько функций. Он должен обеспечивать адекватную прочность и жесткость, чтобы имитировать механические свойства отсутствующей или поврежденной костной ткани.
Важнее всего, что успешный каркас должен стимулировать не только врастание новой ткани, но также прогрессивное созревание и ремоделирование, обеспечивая адекватную поддержку и морфологию. Его конструкция должна учитывать кинетику деградации и физико-химические особенности происходящих в ткани процессов.
Наноматериалы в стоматологии и челюстно-лицевой хирургии
Наноматериалы по сравнению с традиционными материалами обладают такими особенностями, как квантовый размер, макроскопическое квантовое туннелирование, а также небольшие размерные эффекты, приводящие к изменению физико-химических свойств.
Текущие области исследований нанотехнологий для регенерации тканей включают:
-
Методы доставки биоактивных молекул на основе наночастиц.
-
Мечение и наведение веществ на клетки, опосредованные наночастицами.
-
Изготовление материалов для костной пластики на основе наночастиц.
Период полураспада и распределение наночастиц может зависеть от их размера. Их поверхностные свойства определяют стабильность и особенности локализации в тканях. Уменьшение размера частиц наноматериалов выгодно с точки зрения жесткости, эффективной площади поверхности и отношения площади к объему.
Заряд наночастиц также является другим важным фактором, влияющим на интернализацию наноразмерных частиц в различные клетки-мишени. В стоматологии и ЧЛХ применение нанотехнологий в основном сосредоточено на процедурах по восстановлению объема или регенерации костной ткани, а также улучшения остеоинтеграции имплантатов.
Естественная костная ткань образуется высокоорганизованным внеклеточным матриксом (ЕСМ) в нанометровом масштабе, поэтому применение нанокаркасов (nanoscaffolds) может представлять преимущество при увеличении альвеолярного отростка.
Наноматериалы способны преодолеть проблемы, с которыми сталкиваются современные каркасы для регенерации костной ткани, такие как недостаточная механическая прочность, нестабильность высвобождаемых молекул и нарушение дифференцировки.
Обоснование нанотехнологических каркасов в тканевой инженерии
Передовые материалы играют решающую роль в продвижении практического применения технологий тканевой инженерии. На прямое применение терапевтических веществ влияют некоторые ограничения обычных материалов каркаса, включая неспецифическое нацеливание, недостаточную физиологическую стабильность и низкую проницаемость клеточной мембраны. Обычно необходимы сверхфизиологические дозы, чтобы компенсировать плохую фармакокинетику таких агентов, однако это увеличивает потенциальный риск побочных эффектов.
В настоящее время нанотехнология позволила производить структуры, имеющие тот же размер, что и естественные ткани, открыв новую эру для TE / RM.
Нанокаркасы могут изготавливаться таким образом, чтобы они были максимально похожи на тканеспецифичный внеклеточный матрикс. Размер наночастиц позволяет быстро реагировать на внешние раздражители, поступающие из окружающей среды, такие как ультразвук, магнитные поля, pH и воздействие рентгеновских лучей.
Материалы нанокаркаса можно использовать для доставки лекарств, генетического материала или биологических факторов контролируемым образом — причем как системным путем, так и локально. Эти материалы могут стабилизировать активные агенты посредством инкапсуляции или поверхностного прикрепления, способствуя интернализации молекул, направляя их доставку и даже позволяя контролировать высвобождение биологического фактора в намеченную клетку-мишень.
Контролируемая и устойчивая доставка наночастиц в основном зависит от их подходящего размера и соответствующей высокой удельной площади поверхности. Таким образом, наноматериалы могут представлять собой чувствительные к стимулу средства доставки химически или биологически активных веществ в ответ на внешний стимул.
Нанокаркасы отличаются значительной способностью нести лекарственные молекулы, высокой подвижностью частиц и высокой реакционной способностью in vivo по отношению к близлежащим тканям. Их можно использовать для маркировки клеток, чтобы обеспечить непрерывное их отслеживание и мониторинг. Кроме того, наночастицы могут обеспечивать усиленную остеоинтеграцию, остеокондукцию и остеоиндукцию.
Нановолокнистые каркасные системы представляют собой чрезвычайно тонкие непрерывные волокна со значительным отношением площади поверхности к единице массы и высокой пористостью. Пористая структура нановолоконных систем доставки лекарств сильно взаимосвязана и представляет собой адекватный субстрат для клеточной адгезии и транспорта питательных веществ в клетки-мишени.
Волокнистые нанокаркасы, помимо их важной роли в качестве носителей лекарств, обеспечивают механическую прочность. Были опасения, что включение препаратов в нановолокна может ухудшить механические свойства тех же нановолокон.
В качестве примера решения этой проблемы Ionescu и соавторы разработали наполненную микросферами волокнистую структуру, при которой микросферы должны были доставлять лекарства, тогда как нановолокна работали только как механическая поддержка.
Наносферные каркасные системы могут доставлять лекарственные вещества, факторы роста или генетический материал. Преимущества наносфер перед обычными монолитными объемными каркасами можно перечислить следующим образом:
-
Механически слабые каркасы при поддержке напряженных участков могут быть усилены добавлением наносфер в качестве сшивающих агентов.
-
Традиционные каркасы могут быть слишком пористыми, поэтому им требуется механическое усиление добавлением наносфер.
-
Наносферы могут стимулировать образование кристаллов апатита и последующую минерализацию гидрогелей за счет высвобождения соответствующих минералов, так что могут производиться самотвердеющие биоматериалы, адаптированные к регенерации костной ткани.
Инъекционные и / или формованные наноматериалы обладают такими свойствами, что их клиническое применение возможно с помощью минимально инвазивной хирургии.
Классификация наноматериалов для применения в стоматологии
Наноматериалы могут быть неорганического и органического происхождения. Их ассортимент постоянно расширяется. Современная классификация выглядит так:
Синтетические полимеры
Синтетические полимеры имеют такие преимущества, как высокая доступность, простота производства, простая адаптация, профиль безопасности и разумные затраты. Они обладают регулируемыми физико-химическими и морфологическими свойствами. Наиболее распространенными синтетическими полимерами для биомедицинских применений являются полигликолевая кислота, (PGA), полимолочная кислота (PLA), PLGA и поликапролактон.
Керамические материалы
Керамические материалы — это синтетические кристаллические твердые неорганические неметаллические вещества. Биокерамика включает биоактивное стекло, биоактивное стекло-керамику, группы фосфата кальция и оксид алюминия.
Биокерамика обладает такими преимуществами, такими как биосовместимость, нетоксичность и стабильность размеров. Ее добавляют к каркасам для улучшения их структурных свойств и доставки веществ. Некоторые керамические материалы, такие как кальций-фосфатные группы и минеральные триоксидные агрегаты, использовались и в настоящее время используются для увеличения альвеолярного отростка.
Кремниевые наноматериалы
Кремний, сам по себе или в качестве покрытия из других веществ, используется в биомедицинской области, включая визуализацию и доставку лекарств. В соответствии с целями применения наночастицы кремния могут быть синтезированы в виде объемных частиц, двухслойных наночастиц ядро / оболочка и мезопористых наночастиц (MSNP).
Последние обладают высоким потенциалом для применения с практической стоматологии и челюстно-лицевой хирургии. MSNP имеют уникальную пористую структуру, большую площадь поверхности и большой объем пор. Благодаря уникальному строению, напоминающему пчелиные соты, эти частицы способны инкапсулировать и абсорбировать ряд биомолекул для последующей доставки в костную ткань. Их недостаток — потенциальная токсичность.
Металлические наноматериалы
Металлические наночастицы — это биосовместимые материалы с пониженной цитотоксичностью. Их функционализация проста, однако они нуждаются в долгосрочном тестировании на цитотоксичность, и большинство исследователей рекомендуют защищать металлические наночастицы инертными покрытиями.
В биомедицинских целях НЧ золота считаются самыми безопасными и наиболее часто используемыми среди других. Эти наночастицы можно синтезировать в виде сфер, стержней либо решеток, и они могут применяться в таких областях, как доставка лекарств, тестирование на биочувствительность, биовизуализация и фототермическая терапия. Комбинации наночастиц золота и серебра с хитозаном для увеличения альвеолярной кости были описаны с успешными результатами в отношении повышения минерализации и остеоинтеграции имплантата.
Магнитные наноматериалы
В стоматологической практике будущего никель, железо, кобальт и их оксиды будут использоваться в качестве магнитных наночастиц для доставки лекарств, трехмерной организации клеток, мониторинга, визуализации и в качестве биосенсоров.
Некоторые магнитные наночастицы обладают суперпарамагнитными свойствами с возможностью длительного и неинвазивного отслеживания состояния клеток и сред. Однако магнитные наночастицы цитотоксичны, и покрытие необходимо из соображений безопасности и достижения биосовместимости магнитных НЧ.
Липосомальные частицы
Липосомы относятся к органическим частицам. Это везикулы, состоящие из бислоев фосфолипидов. На их свойства влияют размер липидов, поверхностный заряд, состав и метод производства. Липосомы биоразлагаемы, чувствительны к раздражителям и могут быть включены в состав гидрофильных и гидрофобных препаратов.
Они в основном используются для доставки лекарств и визуализации. Это наиболее клинически изученные наносистемы с несколькими известными коммерческими составами. На данный момент основной проблемой является быстрое выведение лизосом из организма, наряду с техническими проблемами их производства и модификации.
Натуральные полимерные материалы
Природные полимеры — это биосовместимые и биоразлагаемые материалы с объемными физическими свойствами. Они делятся в основном на белки и полисахариды. Сюда входит коллаген, альгинат, фибрин, желатин и хитозан. Способы синтеза могут быть гибкими, а полимерные цепи могут демонстрировать большое разнообразие состава и свойств. Как правило, они обладают высокой способностью доставки лекарственных препаратов.
Углеродные нанотрубки
Углеродные нанотрубки представляют собой наночастицы с удлиненной цилиндрической структурой. Это могут быть одностенные или многостенные полые трубчатые конструкции из графита. Они отличаются механической и химической стабильностью наряду с оптимальными электрическими свойствами. Однако химическая стабильность может представлять собой недостаток для процесса функционализации.
Углеродные нанотрубки эффективны при восстановлении костной ткани, поскольку они способствуют пролиферации клеток и остеогенной дифференцировке. Некоторые углеродные наноматериалы, такие как оксид графена (GO), фуллерены, углеродные точки (CD), наноалмазы и их производные, изучаются в инжиниринге костной ткани
Особенности композитных каркасов
Вдохновленные природным составом кости, различные комбинации органических и / или неорганических частиц были протестированы в качестве композитных каркасов, которые усиливают преимущества и уменьшают недостатки каждого компонента.
Чтобы преодолеть недостатки мономатериалов и обеспечить комплексное действие материала при увеличении альвеолярного отростка, созданы различные конструкции композитных каркасов, содержащих природные и синтетические вещества.
Такие конструкции могут состоять из комбинации гидроксиапатита с полимерами высокой молекулярной массы. PLA, PLGA, коллаген, полиамид, кораллин, хитозан и PCL в сочетании с гидроксиапатитом улучшают биосовместимость и механическую прочность каркаса.
Несколько зарубежных исследований по регенерации костной ткани в стоматологии показали, что комбинация гидроксиапатита и коллагеновых каркасов дает наиболее благоприятные механические свойства. Коллагеновое волокно обеспечивает остеоиндуктивный и абсорбируемый каркас для инфильтрации клеток остеобластов, но гидроксиапатит может уменьшить этот эффект. По этой причине процентное содержание ГАП и коллагена в композитных материалах играет решающую роль.
Применение новых материалов для увеличения альвеолярного отростка
В TE / RM одной из основных тем исследований является создание биоконструкций, которые способны интегрироваться с тканями in vivo. Современные системы имеют ограничения, такие как ограниченная диффузия и неравномерное распределение клеточного матрикса. Чтобы преодолеть ограничения существующих материалов, в последние годы были разработаны и испытаны различные типы каркасов.
Регенерация тканей ротовой полости является крайне сложной задачей, и наноматериалы могут представлять большой потенциал для будущего применения при различных черепно-лицевых и оральных дефектах, включая аугментацию альвеолярного отростка.
К наиболее изученным наноматериалам для стоматологии и ЧЛХ сегодня можно отнести нановолокна, наночастицы, нанолисты, нанотрубки и наносферы. Недавно появились также публикации по многослойным нанопокрытиям для регенерации костной ткани.
В целом, наноматериалы обладают превосходными физико-химическими и биомиметическими свойствами для усиления роста клеток и регенерации тканей. Благодаря своему размеру, они способны эффективно контролировать скорость высвобождения каждого агента при разрушении матрикса. Кроме того, их можно использовать для доставки терапевтических агентов при восстановлении альвеолярной кости.
Нановолокна представляют собой идеальную среду для миграции клеток из-за их сходства с внеклеточным матриксом и их высокой пористости. Кроме того, нанотрубки и наночастицы могут улучшать химические и механические свойства каркаса, ускорить миграцию и пролиферацию клеток, а также регенерацию тканей.
Хотя применение наноматериалов в TE / RM все еще находится на начальной стадии с многочисленными ограничениями, которые необходимо решить, результаты недавних исследований указывают на их высокий потенциал.
В настоящее время их применение в стоматологических клиниках и центрах челюстно-лицевой хирургии очень ограничено, однако растет интерес к наноматериалам растет.