Использование костных трансплантатов в ортопедической хирургии стало решающим для лечения ряда заболеваний и травм опорно-двигательного аппарата, включая опухоли костей, а также для артропластики коленного сустава или тазобедренного сустава, и далеко за пределами ортопедической сферы, например, в черепно-лицевой хирургии.
Примерно в 10-15% ортопедических процедур, ежегодно проводимых в Соединенных Штатах, используется тот или иной вид трансплантации костно-мышечной ткани. Только в этой стране банки тканей ежегодно поставляют клиникам более 650 тысяч упаковок аллогенного костного материала, не считая ксеногенных и других типов.
В отличие от других органов, таких как сердце, печень или почки и большинство мягких тканей, кость можно обрабатывать различными способами, чтобы материал мог храниться дольше и имплантироваться без предварительных анализов на совместимость.
Костные материалы можно получить как от самого пациента, так и от живых или мертвых доноров, других биологических видов или даже из неорганических биоматериалов.
Несмотря на успешность использования костных трансплантатов в ортопедической хирургии на уровне 85-90% и массовое внедрение новых материалов, очередь пациентов, ожидающих их получения, растет с каждым днем.
При артропластике используются лиофилизированные аллогенные трансплантаты, хотя их доступность очень ограничена и нельзя полностью исключить риск передачи инфекционных заболеваний. С другой стороны, они по-прежнему малодоступны, и все большее внимание привлекают альтернативные биоматериалы из синтетических и животных источников.
В частности, использование лиофилизированной бычьей кости признано подходящей альтернативой со многими преимуществами перед аутологичными и аллогенными костными трансплантатами в силу ее близкой физико-химической и структурной схожести с человеческой костью и практически неограниченной доступности.
Однако «неспецифический» ксенотрансплантат может вызвать неблагоприятные иммунологические и воспалительные реакции. Поэтому были разработаны протоколы физико-химической обработки, чтобы максимально сократить антигенность и превратить кость от крупного рогатого скота в биоматериал для широкого использования в ортопедической хирургии и других областях медицины.
Особенно широко ксеногенные костные материалы сегодня используют в стоматологической практике. Эти материалы признаны одновременно безопасными, клинически эффективными и экономически доступными для большинства пациентов.
Необходимо расширять знания о свойствах новых материалов, включая биологические и механические аспекты, источники их получения и долгосрочные результаты применения, поскольку эффективная и своевременная пластика костных дефектов отвечает за значительное улучшение жизни и социальную реинтеграцию больных.
Костные материалы в ортопедической хирургии — далеко не новый вопрос, поэтому очень важно в начале XXI столетия четко понимать стратегию их оптимального использования.
В этой статье представлен краткий обзор костных материалов для артропластики, история, показания к применению, особенности хранения и особенности обработки, а также данные по использованию лиофилизированной кости крупного рогатого скота.
Предыстория костной пластики
Идея пересадки тканей между индивидуумами человеческого рода и даже между индивидуумами отдельных видов очень древняя и относится к ранней христианской эпохе.
Легендарные врачеватели Косма и Дамиан в III-IV веках именовались пионерами костной трансплантации, якобы удалившими ногу человека из-за опухоли и пересадив новую ногу.
Однако именно сэр Уильям Макэван в 1880 году успешно восстановил плечевую кость мальчика с помощью кости голени, полученной от другого ребенка. Первая межвидовая пересадка была проведена голландским хирургом ван Мекереном еще в 1668.
По словам Годвина, ему удалось пересадить часть черепа собаки в травматический дефект черепа солдата. Обеспокоенный отлучением его от церкви за нехристианский метод лечения, солдат попросил хирурга удалить трансплантат, но из-за длительного пребывания в организме собачья кость почти полностью интегрировалась.
Неизвестно, когда начались первые исследования костных трансплантатов.
Однако Олье и Барт в конце XIX века первыми сообщили о биологических свойствах костных тканей и пришли к выводу, хотя и верному лишь частично, что кость и надкостница остаются жизнеспособными при трансплантации, способствуя образованию новых костей.
Олби (Albee) в 1915 году в классической работе делает вывод, что наиболее подходящими для трансплантации могут быть ткани, происходящие из соединительной ткани, такие как кость, жир и фасция.
Десять лет спустя, в 1925 году, Лексер опубликовал свой уникальный опыт трансплантации ткани и протезирования суставов, впервые названный словом «артропластика».
Биологические свойства костных материалов для артропластики
Костная ткань в основном состоит из органического матрикса коллагена I типа, содержащего протеогликаны с низкой молекулярной массой и неколлагеновые белки, минеральной части (в основном гидроксиапатита) и воды, что составляет 25, 65 и 10% массы соответственно.
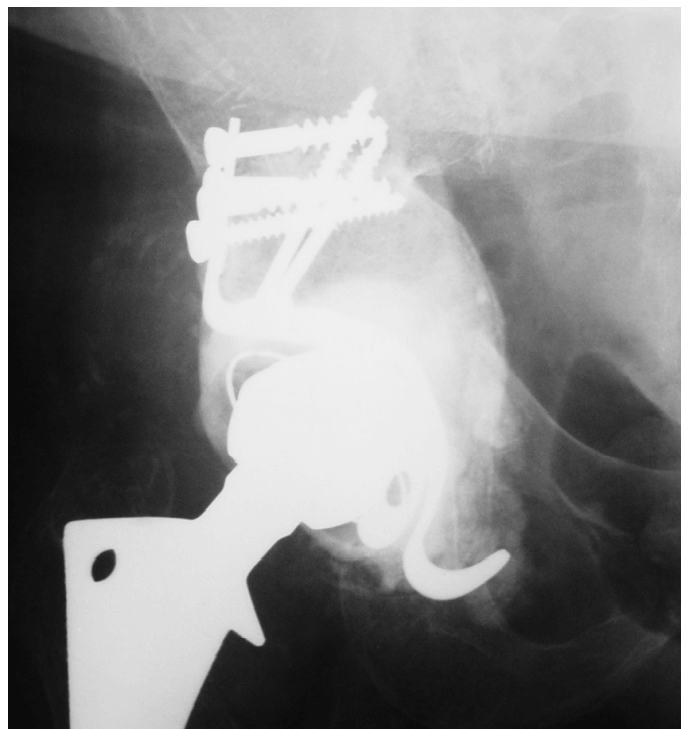
Несмотря на огромную способность к восстановлению, кость не всегда реагирует должным образом при обширном остеолизе. Из-за этих ситуаций, крайне частых в ортопедической хирургии, особенно при ревизионной артропластике тазобедренного сустава, во всем мире существует интерес к поиску высококачественных костных трансплантатов или биоматериалов для восстановления утраченной кости.
Костные материалы могут быть кортикального, губчатого или кортико-антилляционного типа, в зависимости от места происхождения. Эти продукты могут поставляться блоками, чипсами, крошкой или кортикальными фрагментами кости.
Различные типы костных материалов при внесении в организм реципиента инициируют выраженные механические и биологические реакции. Например, кортикальная кость менее остеогенная, чем губчатая, но демонстрирует более высокое структурное качество на протяжении длительного времени и даже при отсутствии адекватной интеграции.
Более высокие остеогенные свойства губчатой кости признаются западными хирургами на протяжении более чем 45 лет, что стимулировало ее использование во многих клинических ситуациях, включая ревизионную артропластику тазобедренного сустава.
После трансплантации губчатой кости возникает каскад гистологических реакций, который начинается с острого воспалительного ответа, инвазии макрофагов, неоваскуляризации и дифференцировки мезенхимальных клеток в остеобласты, формирующих остеоидный слой в остатках некротизированной костной ткани.
Все эти события, вероятно, опосредованы индуцирующими белковыми факторами.
В исследовании Buma и соавт. была проведена гистологическая оценка состояния костной ткани у восьми пациентов, которые перенесли ревизию ацетабулярного компонента после операции с применением костной пластики.
Все образцы, кроме одного, в котором признаки реваскуляризация отсутствовали, показали различные стадии интеграции в зависимости от времени, прошедшего после имплантации.
Через 4 месяца происходила реваскуляризация, остеобласты заменяли части имплантата, оставалось небольшое количество трансплантата и нового костного образования. Образцы с более длительной эволюцией продемонстрировали, что внесенный костный материал постепенно заменяется новой костью (см. иллюстрацию).
Аналогичные результаты по бедренной составляющей были продемонстрированы в другом исследовании, опубликованном Ульмарком и Обрантом в 2002 году, а также Galia и соавт. при биопсии вертлужной впадины у ряда пациентов с травматическим смещением после ревизионной артропластики тазобедренного сустава.
В классическом исследовании Urist описал эктопический остеогенез при внутримышечной имплантации деминерализованного костного матрикса у кроликов и крыс. Данное открытие имело решающее значение в области новых биоматериалов и трансплантологии и способствовало поиску веществ, способных индуцировать дифференцировку клеток, присутствующих в костном матриксе человека.
Последующие исследования под руководством Urist и соавт. показали, что низкомолекулярные белки могут быть извлечены из деминерализованного костного матрикса. Эти вещества, обладающие высокой остеогенной активностью и называемые костными морфогенетическими белками (ВМР), принадлежат к суперсемейству белков, трансформирующих факторов роста-бета (TGF-ß).
Суперсемейство белков TGF-ß регулирует многие жизненно важные биологические процессы, включая рост клеток, дифференцировку и формирование эмбрионов.
Доказано, что ВМР являются важными регуляторами в развитии и регенерации скелетной ткани, причем наибольшим остеоиндуктивным потенциалом обладают ВМР-2 и ВМР-7.
Другим важным фактором является реакция, вызываемая антигенными трансплантатами.
Антигены, присутствующие в клетках костного материала, вероятно, играют очень важную роль в результатах костной пластики как таковой. Понятно, что такие реакции протекают не через Т- или В-лимфоциты, а через другие клетки костного мозга.
Данные in vitro свидетельствуют, что линии гранулоцитов в костном мозге вызывают иммунный ответ и, следовательно, удаление клеток костного мозга, способно оказать воздействие на иммунный ответ организма против трансплантата.
Исследователи экспериментально сравнивали свежие, замороженные и лиофилизированные костные трансплантаты у кроликов с иммунологической позиции. Первые два трансплантата вызвали серологически определяемый иммунный ответ, а третий, высокоочищенный (свободный от жировых и костных клеток), не способен иммунологически сенсибилизировать лабораторных животных.
Хотя лиофилизированные костные материалы для артропластики и ортопедической хирургии широко доступны в медицинских центрах по всему миру, большинство исследований по ревизионной артропластике тазобедренного сустава относится к использованию замороженных костных блоков или же кортикальных фрагментов кости.
Tagil и соавт. в своем исследовании 2000 года попытались объяснить причины успеха использования измельченных костных материалов. Они обнаружили ряд возможностей:
-
Измельчение кости, как и при оскольчатом переломе, способствует значительному увеличению площади поверхности, обеспечивая доступ и высвобождение большего количества биологически активных веществ и ростовых факторов.
-
Удары могут улучшить остеокондуктивные свойства материала, что приведет к высвобождению ВМР и тем самым будет способствовать остеоинтеграции.
-
Повышенная эластичность может привести к появлению мелких деформаций, способствующих образованию новых костей.
Важность этого исследования заключается в том, что для прогнозирования клинического результата с научной точки зрения важно знать все "за" и "против" техники производства конкретного костного материала.
Механические свойства костных материалов для артропластики
В дополнение к биологическим характеристикам, механические аспекты очень важны и могут быть решающими при выборе костного трансплантата для той или иной процедуры.
Итаман и Накамура в 1991 году исследовали гистологические и биомеханические аспекты различных способов обработки костного трансплантата крыс и отметили резкое повышение жесткости материала после замораживания при -80°C и лиофилизации.
Лиофилизированная деминерализованная кость, подвергшаяся сублимационной сушке, первоначально потеряла свою механическую прочность. Но через 16 недель наблюдалось постепенное повышение прочности, что может быть связано с биологическим взаимодействием и является индикатором остеоиндуктивных свойств.
Японские исследователи также пришли к выводу, что аутологичная кость, как и предполагалось, демонстрирует более высокую степень интеграции.
Физические свойства губчатой кости человека и крупного рогатого скота документально подтверждены, однако разброс экспериментальных результатов очень широкий.
Модуль Юнга, например, в одном исследовании составлял от 70 до 673 МПа, а прочность на сжатие варьировалась от 2,44 до 6,24 МПа. Такой разброс характеристик относится и к кости человека, и к ксеногенным костным материалам.
Неоднородность полученных результатов может быть связана с несколькими факторами, включая возраст донора, плотность кости, методы получения материала и измерения.
Между тем, разница в ожидаемых механических свойствах кости в 3-10 раз может представлять серьезную проблему при лечении нагруженных участков скелета.
Cornu и соавт. в 2001 году продемонстрировали in vitro, что лиофилизированная измельченная кость механически превосходит замороженную кость, и авторы называют причиной, что лиофилизированный костный материал лишен жира и костного мозга.
В 1999 году Македо, используя автоматизированную компрессионную машину, сопоставлял in vitro прочность замороженной и лиофилизированной кости крупного рогатого скота, подвергавшейся регидратации в течение часа. Автор обнаружил, что данные материалы имеют схожие характеристики и скорость деформации с регидратированной лиофилизированной костью крупного рогатого скота.
Методы стерилизации, инфекционные заболевания и безопасность
Чрезвычайно важным вопросом является изучение методов стерилизации замороженных и лиофилизированных костных материалов, поскольку здесь все еще остаются противоречия и необходимость проведения дальнейших исследований.
Доступные в настоящее время методы имеют преимущества и серьезные недостатки, касающиеся эффективности и сохранения механических и биологических свойств.
Сообщалось о вредном воздействии кобальта-60 при стерилизации лиофилизированных трансплантатов, демонстрируя, что даже при низких дозах радиация способна нарушать морфогенетические свойства, главным образом, в недеминерализованной кости.
Воздействие радиации на биомеханику костных трансплантатов зависит от дозы.
Фиделе в 1995 году изучал ущерб, нанесенный применением разных доз гамма-излучения замороженной аллогенной костной ткани надколенника по 7 биомеханическим параметрам.
Например, стерилизующая доза для инактивации ВИЧ составляет около 25 кГр.
Однако четыре из семи измеренных параметров были значительно ухудшены после облучения дозой 20 кГр, а после 30 кГр все параметры показали снижение.
Чжан и Деллой в 1997 году в экспериментальном исследовании на крысах сравнивали остеоиндуктивные свойства трансплантата после стерилизации гамма-излучением (25 кГр), этиленоксидом при 55°С и 40°С или обработки этанолом.
Эксперименты показали, что этиленоксид при 40°C и этанол не оказывают отрицательного влияния на остеоиндукцию, гамма-излучение снизило ее на 40%. Обработка этиленоксидом при температуре 55°C почти полностью разрушило этот потенциал.
Некоторые авторы указывают на другие факторы стерилизации, которые необходимо контролировать. В том числе потенциально токсичные остатки этиленоксида, которые остаются в материале и высвобождаются при контакте с жидкостями тела.
Также следует рассматривать токсичность гамма-излучения при контакте с жиром, присутствующим в костной ткани. Этот негативный эффект дополняет физические изменения, которые может вызвать излучение.
Другой способ стерилизации — автоклавирование кости, хотя у него есть ограничения.
В соответствии с рекомендацией ЕС, направленной на инактивацию прионов (инфекционных белки), ткани коровьего происхождения стерилизуют в автоклаве при 132°С в течение 1 часа, но биомеханические эффекты этого метода стерилизации проявляются снижением приблизительно на 70% механической устойчивости материала к сжатию.
Многие авторы поддерживают безопасность нестерилизованных костных трансплантатов, предоставленных банками, которые применяют соответствующую методологию для отбора доноров и контроля качества. Контроль настолько важен, что при применении данных критериев отбраковывают от 20% до 30% собранного материала.
Основной причиной отбраковки костного материала являются неудовлетворительные бактериологические или серологические результаты.
Несмотря на этот строгий контроль, в ноябре 2001 года в США было зарегистрировано два случая инфекции Clostridium sordellii у хирургических пациентов после костной пластики.
В марте 2002 года Центр по контролю и профилактике заболеваний США получил 26 подтвержденных сообщений из разных мест о вторичных бактериальных инфекциях в трансплантированных костно-мышечных тканях.
В этих случаях CDC исследовал доноров и подтвердил присутствие этих бактерий в их тканях. Только в США ежегодно поступают десятки сообщений об инфекционных агентах, передаваемых при использовании аллогенного костного материала в ортопедической хирургии, стоматологии, нейрохирургии и др.
Все это требует еще более строгого контроля, пересмотра принятых процедур и, возможно, поиска методов стерилизации, которые минимально влияют на эффективность материала.
Тейлор в 2002 году заявил, что прионы, ответственные за болезнь Крейтцфельдта-Якоба у людей и губчатый энцефалит крупного рогатого скота, в отличие от бактерий и вирусов, устойчивы к таким процедурам, как автоклавирование или воздействие гидроксида натрия.
Но добавление щелочных веществ и нагревание даже при 100°C на протяжении 1 минуты оказывается эффективным для инактивации прионов. Обработка материала гипохлоритом натрия также демонстрирует способность инактивировать прионные белки.
Потенциально опасные вирусные заболевания, такие как гепатит A, B или C, ВИЧ и Т-лимфотропный вирус человека, а также другие недавно выделенные вирусы и некоторые типы опухолевых клеток вызывают у специалистов беспокойство.
Даже с учетом современных знаний и осторожности в плане серологических и других диагностических методов, эти возбудители продолжают представлять угрозу.
Sugihara и соавт. в 1999 году провели гистологическое исследование ткани 137 головок бедра, полученных при тотальной артропластики тазобедренного сустава. Авторы выявили высокий процент гистологических нарушений и опухолевые клетки, что подчеркивает важность тщательного гистопатологического исследования донорских тканей.
Хранение и обработка костных материалов
Банки по всему миру используют разнообразные способы обработки и хранения костной ткани для клинического применения. Среди них мы выделяем глубокой заморозки (-80oC) и лиофилизации, которые являются наиболее широко используемыми и общепринятыми.
Глубокая заморозка достигается в морозильных камерах, температура которых достигает -80oC, и поддерживается стабильной благодаря электронным системам, контролирующим температуру, имеющим собственные генераторы энергии и аварийные сигналы, оповещающие о повышении температуры.
Таким образом, после тщательного отбора доноров (живых или мертвых), серологических тестов и посева на бактерии и грибки, а также соответствующей обработки, трансплантаты подвергают замораживанию при, что позволяет хранить их до 5 лет.
Низкие температуры не играют никакой роли в стерилизации материала, но действительно снижают антигенность, обеспечивая более высокую безопасность при использовании.
Лиофилизация, предложенная и внедренная в 1951 году Банком тканей ВМФ США, представляет собой метод, с помощью которого достигается обезвоживание материала. Этот материал проходит процесс промывки, центрифугирования, децеллюляризации, физической стерилизации и очистки с сохранением только белково-минерального матрикса с минимальной антигенностью.
Лиофилизация представляет собой удобный способ обработки и хранения тканей опорно-двигательного аппарата. Лиофилизация применяется не только для человеческой костной ткани, сухожилий и фасций (аллогенных), но и для тканей крупного рогатого скота (ксеногенных), обеспечивая совместимость за счет снижения антигенности.
В настоящее время в крупных медицинских центрах западных стран доступны различные типы костных материалов для реконструктивной ортопедической хирургии: замороженная и лиофилизированная аллогенная, аутологичная и ксеногенная кость.
Аутологичный трансплантат не требует многоступенчатой обработки и рассматривался с точки зрения интеграции как наиболее предпочтительная ткань для замены кости.
Имеется информация, что выживание остеобластов и остеоцитов из аутологичного трансплантата зависит от качества ложа рецептора. Помимо этого недостатка, количество получаемой аутокости ограничено лечением мелких дефектов, а вероятность местных и системных осложнения во время получения ткани составляют 21-49%.
Замороженный аллогенный трансплантат является наиболее широко используемым и общепринятым в настоящее время, но он не всегда доступен в больших количествах.
Несмотря на все принятые банками стандарты по уходу и биобезопасности, все еще существует определенный риск передачи инфекционных заболеваний и опухолей.
Ксеногенные костные материалы для артропластики, хорошо известные стоматологам, начинают все более активно использоваться в ортопедической хирургии на Западе, особенно костная ткани бычьего происхождения. Причина заключается в доступности, высоком сходстве с человеческой костью, эффективностью и простотой подготовки.
Бычья кость имеет химический состав, пористость, размер, форму и биологическое поведение, аналогичные человеческому аналогу. Помимо этих особенностей, бычий трансплантат обеспечивает структурную поддержку, остеокондукцию и высокое содержание кальция и фосфора — все это существенные факторы для новообразованной костной ткани.
Самой важной проблемой, независимо от типа выбранного материала, является гарантия того, что он обрабатывался и хранился в соответствии с действующими стандартами.
Заключение
Среди костных материалов для артропластики в ортопедической хирургии активно используются и аутологичная, и аллогенная, и в последнее время ксеногенная кость. Существует масса различий между этими продуктами, включая метод обработки, производства, форму выпуска (чипсы, крошка, блоки) и т. д.
Хотя эти материалы применяют в клинической практике на протяжении десятилетий, ряд механических и биологических проблем, таких как физико-химический состав, включение, ремоделирование кости и иммунные реакции, все еще не полностью изучены.
Нуждаются в совершенствовании методы обработки и стерилизации материалов, которые позволят получать надежный и готовый к использованию продукт с нужными свойствами.
Нет сомнений в важности костной пластики для ортопедической хирургии, особенно в артропластике тазобедренного сустава. Ее результаты хорошо известны и, в некоторой степени, предсказуемы, если процедуры выполняют опытные хирурги.
К сожалению, наука все еще мало знает об аспектах взаимодействия трансплантат-хозяин. Например, почему 85% трансплантатов теоретически интегрируются? Хотя это покажется хорошим процентом, как насчет других 15% «не очень удачных» случаев? Это вопрос техники, иммунного ответа, механического или же биологического воздействия?
Какой лучший заменитель аутологичной костной ткани? Замороженный аллогенный трансплантат? Облученный или автоклавированный? Это лишь некоторые из важных, но оставшихся без ответа вопросов, которые придется тщательно изучать и анализировать.

